Bonjour les amis chimistes (ou dirais-je Pierre et Blackline ?  ) !
) !
La semaine prochaine je synthétise le cisplatine, un fameux composé anticancéreux. La voie de synthèse la plus communément effectuée est celle-ci:
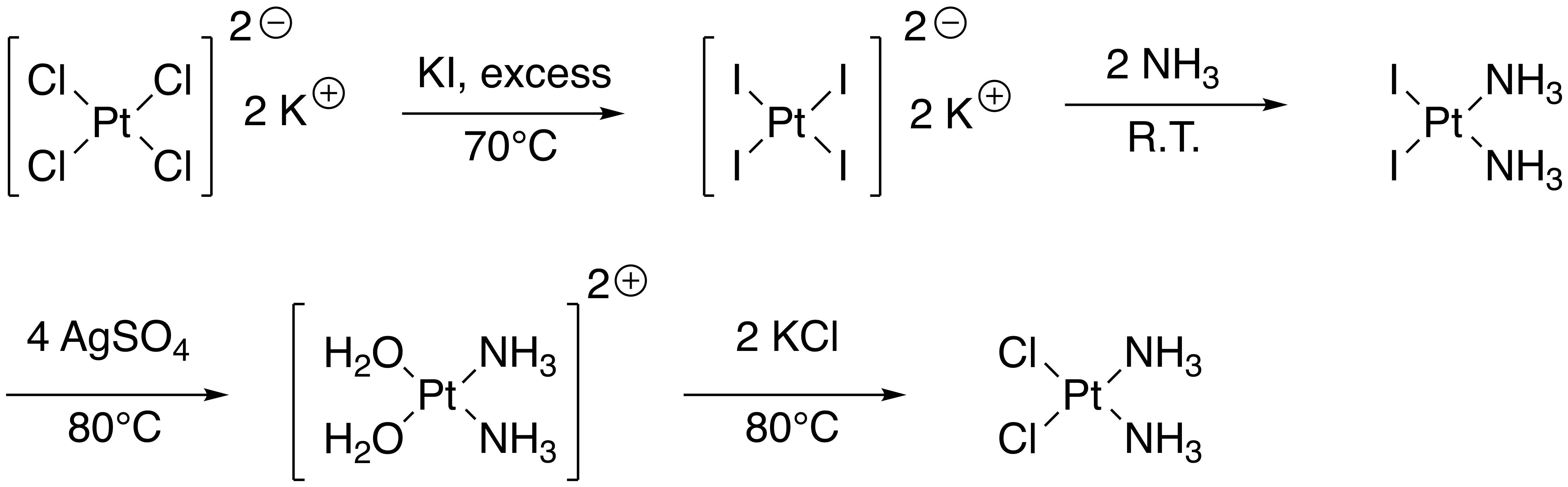
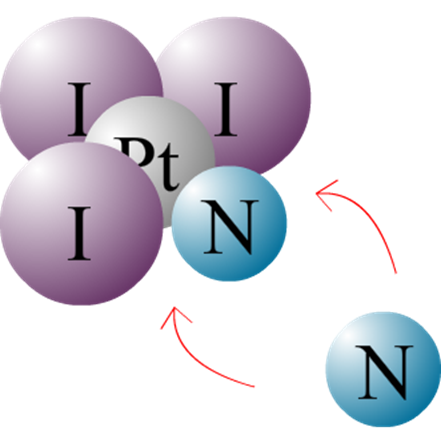
Dans mon protocole de laboratoire, on me parle donc de cet effet trans. Si j’ai bien compris, l’effet trans est le fait qu’un nouveau ligand va se lier en trans d’un ligand en particulier et différents ligands sont classés suivant une table. Comme l’iode a un effet trans plus important que celui du chlore favorise la synthèse du cisplatine, car le deuxième NH3 va se mettre en trans de l’iode.
Le problème c’est que je comprends pas vraiment pourquoi (d’un point de vue quantique / orbitalaire) et je sais pas s’il y a de la documentation là dessus car j’ai pas trouvé. Je suppose que ça doit être dû à la meilleure polarisabilité de l’iode et de sa facilité à accepter toute la densité électronique provenant du platine (grâce à sa haute électronégativité). Mais ça reste des explications assez floues et je suis pas sûr 
Je suppose qu’on a tout de même formation des deux configurations cis et trans mais simplement avec un cis largement majoritaire.
Merci d’avance!