À la fin du précédent chapitre nous vous avions dit que le cyanure pouvait également réduire l’absorption intestinale de glucose ainsi que l’oxygénation des tissus. Certes ce ne sont pas ces deux effets qui permettent d’expliquer la mort mais ils existent quand même et constituent un facteur aggravant dans l’intoxication au cyanure. Nous pensons donc qu’il est tout de même important de les présenter. 
À la fin de ce chapitre vous serez en mesure de :
- Comprendre comment le cyanure diminue l’absorption intestinale de glucose ;
- Comprendre comment l’organisme est alimenté en dioxygène avec les bases de la physiologie respiratoire et circulatoire (vous verrez c’est très intéressant au niveau fonctionnel) ;
- Comprendre de ce fait comment le cyanure diminue l’extraction de dioxygène par les tissus.
Sans plus attendre nous vous proposons de commencer par l’absorption intestinale de glucose et le cyanure. Pour une raison simple : cette partie va être rapide puisque nous avons déjà vu comment l’intestin était capable d’absorber le glucose et nous allons nous resservir de cette notion qui est normalement encore toute fraîche dans vos esprits. 
- Le cyanure diminue l'absorption intestinale de glucose
- Le cyanure diminue l'extraction du dioxygène par les tissus
Le cyanure diminue l'absorption intestinale de glucose
Au début du précédent chapitre nous avions étudié les phénomènes de transport du glucose au niveau de l’intestin. Pour rappel le glucose rentrait dans les entérocytes via un transporteur SGLT. Ce transport est qualifié de transport actif secondaire puisqu’il utilise l’énergie contenue dans le gradient électrochimique du sodium (symport sodium et glucose, les deux entrent dans l’entérocyte). Et justement nous avions aussi dit que le transport actif secondaire dépendait du transport actif primaire dans le sens où c’est l’action de la pompe Na+ K+ ATPase qui permet de maintenir une plus grande concentration de sodium dans le milieu extracellulaire. Et cette pompe utilise de l’ATP pour fonctionner.
Vous voyez où nous voulons en venir ? Le cyanure empêche la production d’ATP comme déjà vu précédemment. Donc la pompe Na+ K+ ATPase ne pourra plus (ou beaucoup moins bien) maintenir une plus forte concentration de sodium extracellulaire. Ainsi le transport actif secondaire sera perturbé, les concentrations de sodium intracellulaire et extracellulaire vont s’équilibrer et le flux net de sodium sera nul. Le glucose ne pourra donc plus rentrer dans les entérocytes puisqu’il est plus concentré dans les entérocytes que dans la lumière intestinale et son transport nécessitait ce transport actif secondaire justement !
D’accord. Mais le glucose qui était déjà présent dans l’entérocyte ira dans le sang et finalement, au fur et à mesure du temps, il ne devrait plus en rester dans l’entérocyte. À ce moment précis, le glucose de la lumière intestinale ne pourrait-il pas pénétrer dans les entérocytes même sans transport actif secondaire ?
C’est bien vu, très bien vu même ! Si vous vous êtes posé la question seul cela montre que vous commencez à très bien maîtriser le sujet. Sinon aucune inquiétude, vous êtes là pour en savoir plus justement.  Pour répondre à cette question il faut savoir que nous vous avions volontairement caché quelque chose (eh oui encore). En fait les entérocytes possèdent bien le transporteur SGLT mais également un transporteur GLUT qui pour rappel permet le passage du glucose selon son gradient de concentration (donc du milieu où il est le plus concentré vers celui où il est moins concentré).
Ce transporteur GLUT n’est pas seulement à l’autre bout de la cellule comme dit dans le précédent chapitre mais peut aussi être retrouvé sur la même face de la cellule où est retrouvé le transporteur SGLT.
Pour répondre à cette question il faut savoir que nous vous avions volontairement caché quelque chose (eh oui encore). En fait les entérocytes possèdent bien le transporteur SGLT mais également un transporteur GLUT qui pour rappel permet le passage du glucose selon son gradient de concentration (donc du milieu où il est le plus concentré vers celui où il est moins concentré).
Ce transporteur GLUT n’est pas seulement à l’autre bout de la cellule comme dit dans le précédent chapitre mais peut aussi être retrouvé sur la même face de la cellule où est retrouvé le transporteur SGLT.
Nous vous avons remis l’image du chapitre précédent pour plus de clarté (qui ne montre pas la présence du transporteur GLUT sur la même face que le transporteur SGLT, mais cela existe, nous vous l’assurons  ) :
) :
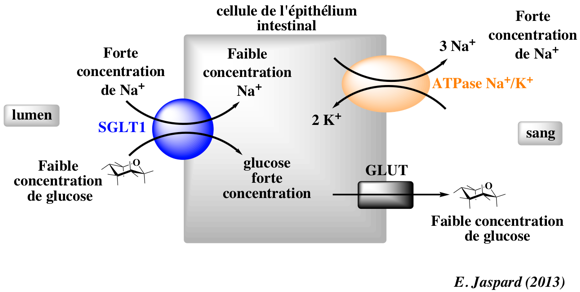
Donc la réponse à la question est oui, en présence de cyanure le glucose pourra tout de même au bout d’un certain temps entrer dans les entérocytes. Seulement son transport sera bien ralenti car il aurait pu déjà y entrer via le transporteur SGLT, sans attendre que le gradient de glucose soit favorable à son entrée dans les entérocytes via ce transporteur GLUT.
De manière plus physiologique, ce transporteur GLUT qui est retrouvé à côté du transporteur SGLT, sert à faire entrer le glucose quand il est plus concentré dans la lumière intestinale que dans les entérocytes. En effet nous ne vous l’avions pas dit (et l’image dit même le contraire ici) mais le glucose n’est pas toujours plus concentré dans les entérocytes que dans la lumière intestinale. Après un repas, surtout très sucré et riche en glucose, le glucose de la lumière intestinale devient plus concentré que dans les entérocytes et peut donc entrer dans les entérocytes sans le transporteur SGLT donc sans transport actif secondaire. Seulement le transporteur SGLT est quand même très utile physiologiquement puisqu’il permet l’entrée de glucose contre son gradient de concentration, même quand le rapport de concentration s’inverse (et Dieu sait que c’est souvent le cas). Cela permet au corps d’être assuré de toujours avoir assez de glucose.
Le cyanure diminue l'extraction du dioxygène par les tissus
En plus de diminuer l’absorption intestinale de glucose le cyanure peut également diminuer l’extraction du dioxygène par les tissus périphériques (principalement les muscles). La grande question c’est comment ? Nous avons vu que la diminution d’absorption intestinale du glucose pouvait finalement s’expliquer par la diminution de production d’ATP en présence de cyanure. Alors comme tout bon scientifique qui se respecte nous allons faire une hypothèse très simple : la diminution d’extraction du dioxygène par les tissus est également due à la diminution de production d’ATP en présence de cyanure.
Et est-ce que c’est vrai ? C’est l’objet de cette partie !
Bon déjà, ce qui nous vient en premier à l’esprit, si on souhaite confirmer ou infirmer cette hypothèse, c’est de faire le parallèle avec le cas du glucose. Rappelez-vous, le glucose est d’abord dans la lumière intestinale avant d’être absorbé pour aller dans le sang. Ensuite il est absorbé par les divers tissus de l’organisme. Et concernant le dioxygène ? Vous avez la réponse. On respire, ce dernier se trouve donc dans les poumons (comme pour l’intestin on va parler de lumière alvéolaire, c’est-à-dire l’intérieur des alvéoles pulmonaires). Ensuite le dioxygène peut gagner le sang et une fois dans le sang pourra être utilisé là aussi par les divers tissus de l’organisme. Si vous suivez toujours, la comparaison avec le glucose doit se faire au niveau du passage alvéoles/sang. Puisque c’est l’équivalent du passage intestin/sang pour le glucose et c’est à ce passage que nous avions expliqué l’effet du cyanure sur la diminution d’absorption intestinale de glucose. Donc pouvons-nous expliquer l’effet du cyanure sur la diminution d’extraction du dioxygène par les tissus en nous concentrant au niveau du passage alvéoles/sang ? Puisque si moins de dioxygène parvient à gagner le sang alors les tissus pourront moins bien tirer le dioxygène dont ils ont besoin pour fonctionner.
Et pour le savoir il semble nécessaire d’étudier le mécanisme de diffusion du dioxygène depuis les alvéoles jusqu’au sang. S’il nécessite de l’ATP c’est gagné puisque le cyanure bloque sa production ! Alors qu’en est-il ?
Le mécanisme de diffusion du dioxygène
Voici une bien belle illustration de l’interface alvéoles/sang aussi appelée interface air/sang.
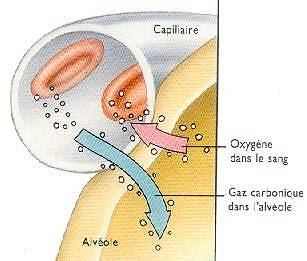
Sur cette image vous voyez que le dioxygène passe des alvéoles vers le sang et le gaz carbonique (le dioxyde de carbone) passe du sang vers les alvéoles pour y être expiré.
Si nous vous donnons cette image ce n’est pas pour rien. Nous n’avions pas envie de vous ennuyer avec des considérations histologiques (étude des tissus) et avec des noms à dormir debout (du type endothélium, interstitium et d’autres, bon ok j’arrête, ne serait-ce que par respect pour les gens dont le travail est d’étudier les tissus  ), du coup nous préférons vous donner une image concrète. Nous préférons évoquer avec vous le côté fonctionnel et ce qui va nous intéresser ici c’est le mécanisme qui permet au dioxygène de passer vers le sang, en particulier s’il dépend de l’ATP.
), du coup nous préférons vous donner une image concrète. Nous préférons évoquer avec vous le côté fonctionnel et ce qui va nous intéresser ici c’est le mécanisme qui permet au dioxygène de passer vers le sang, en particulier s’il dépend de l’ATP.
Pour le savoir intéressons-nous un peu aux membranes plasmiques, c’est-à-dire ce qui délimite une cellule de son environnement. Dans notre cas la cellule qui borde les alvéoles est une cellule épithéliale, par exemple un pneumocyte (pour faire le lien avec l’intestin, l’équivalent était l’entérocyte). La membrane plasmique du pneumocyte délimite donc le pneumocyte de l’air contenu dans les alvéoles. Voici une image d’une membrane plasmique :
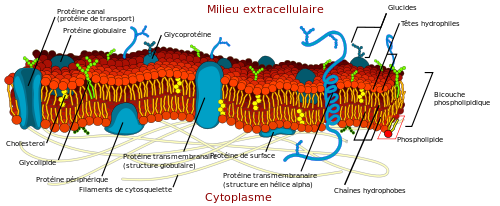
La membrane plasmique a plusieurs rôles dont celui de protéger la cellule de son environnement. Mais ce qui va nous intéresser c’est la composition de cette membrane. Sur l’image vous voyez des choses bleues aux formes un peu bizarres, on ne va pas s’y intéresser. Retenez simplement que ce sont des protéines ancrées dans la membrane et qui ont plusieurs rôles (par exemple faire passer des ions vers l’intérieur des cellules, mettez ça en lien avec la première partie quand nous parlions des canaux voltage dépendant avec le potentiel d’action). Les transporteurs sont aussi des protéines qui peuvent être retrouvées dans les membranes plasmiques, par exemple SGLT et GLUT pour ce que nous venons de voir au niveau de la membrane plasmique des entérocytes.
Mais sur l’image vous voyez aussi du rouge, surtout du rouge en fait. Et c’est ce qui va nous intéresser maintenant. Ce ne sont pas des protéines mais des lipides (la composante gras de l’organisme pour faire très simple). Et les membranes plasmiques sont composées de lipides particuliers appelés des phospholipides (d’autres lipides comme le cholestérol entrent aussi dans la composition des membranes). Au niveau de la classification il faut savoir que les phospholipides comprennent les phosphoglycérides et la sphingomyéline mais nous allons nous concentrer sur les phosphoglycérides. Au niveau moléculaire un phosphoglycéride c’est ça :
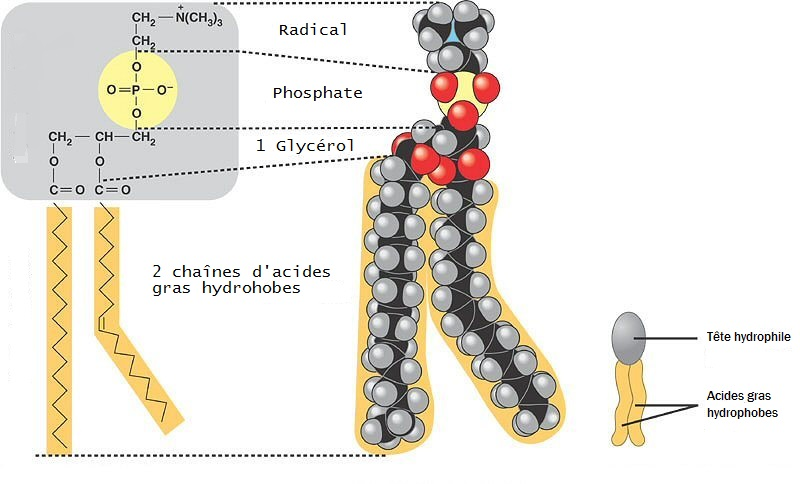
Il faut remarquer que la molécule est organisée autour d’un squelette de glycérol comme indiqué sur l’image. À partir de ce squelette deux molécules d’acides gras sont branchées dessus. Les deux acides gras sont encadrés en orange sur l’image et sont constitués d’un grand nombre d’atomes de carbone. On dit que ces acides gras constituent la partie hydrophobe du phosphoglycéride. Cela signifie que cette partie du phosphoglycéride n’a pas d’affinité avec l’eau et aura tendance à l’éviter. Au contraire la partie du phosphoglycéride contenant le groupement phosphate couplé au radical et que vous voyez également branché au squelette de glycérol est hydrophile. Cela signifie que cette partie de la molécule (indiquée en grise sur l’image) a plus d’affinité avec l’eau. En schématisant le phosphoglycéride peut donc être représenté comme une sorte de bonhomme avec deux jambes (les deux acides gras hydrophobes en orange) et avec une tête grise (la partie hydrophile de la molécule), c’est ce que vous voyez en bas à droite de l’image. On dit aussi que la molécule de phosphoglycéride est amphiphile, c’est-à-dire qu’elle comporte une partie hydrophobe et une autre partie hydrophile.
Nous vous racontons tout ça car cela a une conséquence fonctionnelle directe. Les milieux extracellulaire et intracellulaire sont composés d’eau donc cela signifie que la partie hydrophile du phosphoglycéride va avoir tendance à pointer vers ces milieux avec lesquels elle a de l’affinité. Au contraire les deux acides gras du phosphoglycéride auront tendance à éviter l’eau. Pour cela les deux acides gras ne pointeront pas vers le milieu extracellulaire car composé d’eau. Ils ne pourront pas non plus pointer vers le milieu intracellulaire car également composé d’eau. Mais alors comment vont-ils faire ? Eh bien en réalité deux phosphoglycérides vont s’associer dans une configuration qui va permettre à leurs molécules d’acides gras de minimiser leurs contacts avec l’eau. Pour cela les deux molécules d’acides gras de chacun des deux phosphoglycérides vont se rejoindre pour former une membrane plasmique constituée d’une bicouche lipidique (deux phosphoglycérides se faisant face à face). Le deuxième phosphoglycéride "du bas" aura également sa tête hydrophile orientée vers l’eau du milieu intracellulaire tandis que les deux molécules d’acides gras s’organiseront avec les deux molécules d’acides gras du phosphoglycéride "du haut".
Regardez l’image précédente de la membrane plasmique pour mieux situer tout cela.
Une autre conséquence fonctionnelle très importante, et là c’est ce qui va nous intéresser, c’est que seules les molécules liposolubles, solubles dans les lipides, pourront traverser les membranes plasmiques pour gagner le milieu intracellulaire. Par exemple le dioxygène et le dioxyde de carbone sont liposolubles. Certaines vitamines et les hormones stéroïdiennes sont également liposolubles. Au contraire les espèces chargées comme les ions et d’autres molécules comme l’eau ou le glucose ne sont pas liposolubles et ne pourront donc pas traverser les membranes biologiques sans l’aide de transporteurs ou canaux ioniques particuliers. Vous comprenez maintenant mieux pourquoi nous vous avions raconté tout cela sur les membranes plasmiques. Nos deux gaz d’intérêt, le dioxygène et le dioxyde de carbone, pourront traverser les membranes biologiques sans transporteur particulier, au contraire du glucose par exemple !
C’est-à-dire qu’au niveau de l’interface air/sang dans les alvéoles, le dioxygène pourra passer dans le sang en passant à travers les membranes plasmiques des pneumocytes. Il n’y a donc a priori pas besoin d’ATP dans ce transport du dioxygène ! C’est ce qu’on appelle un transport passif par diffusion simple. Ce transport se fait selon le gradient de concentration, du milieu où le gaz est le plus concentré vers celui où il est le moins concentré. Donc notre hypothèse de départ semble fausse : on ne peut pas expliquer la diminution d’extraction du dioxygène par les tissus par le fait qu’il y ait moins d’ATP en présence de cyanure. Même avec moins d’ATP le dioxygène pourra passer dans le sang et ensuite passer dans les cellules des tissus périphériques également (interface sang/tissus). Donc comment expliquer la diminution d’oxygénation des tissus en présence de cyanure ? Pour le savoir il semble raisonnable de se pencher plus en détails sur la physiologie respiratoire et circulatoire. Nous allons donc commencer par étudier ce qu’il se passe quand nous respirons.
Un peu de physiologie respiratoire…
Avant toute chose commençons au niveau macroscopique. Voici donc une image de ce qu’il se passe quand on inspire et expire :

Cela peut vous sembler évident mais nous allons nous servir de cette image très concrète pour aller ensuite dans le détail fonctionnel des choses et nous avons trouvé que cette image résumait très bien les choses (en plus ça vient d’un site de yoga  ).
Nous allons commencer par voir ce qu’il se passe lors d’une inspiration et ensuite vous comprendrez naturellement ce qu’il se passe lors de l’expiration.
).
Nous allons commencer par voir ce qu’il se passe lors d’une inspiration et ensuite vous comprendrez naturellement ce qu’il se passe lors de l’expiration.
Lors d’une inspiration
S’il y a une seule chose que vous devez retenir pour cette partie c’est la formule suivante :
P représente la pression en mmHg (millimètre de mercure) et V le volume en litre. C’est la loi de Boyle-Mariotte. Vous allez tout de suite voir le rapport avec l’inspiration.
Lors d’une inspiration, comme le montre l’image précédente, le diaphragme va se contracter et s’aplatir. C’est un muscle inspiratoire. D’autres muscles inspiratoires comme les intercostaux externes vont se contracter pour pousser les côtes vers l’avant (ce qui est montré sur l’image avec les flèches). La conséquence de cela c’est que la cage thoracique va augmenter de volume. Et c’est là que la formule précédente intervient. Pour que P*V reste constant, si V augmente alors il faut que parallèlement P diminue. Donc lors de l’inspiration le volume de la cage thoracique augmente et la pression intra-pulmonaire (aussi appelée pression intra-alvéolaire) va diminuer elle.
Il faut savoir que la pression atmosphérique de l’air environnant est de 760 mmHg. Lors de l’inspiration la pression intra-alvéolaire diminue et passe de 760 mmHg à 759 mmHg. Les gaz vont passer du milieu où la pression est la plus forte vers le milieu où la pression est plus faible. Donc lors d’une inspiration l’air va entrer dans les poumons.
C’est ce que vous voyez sur l’image suivante :
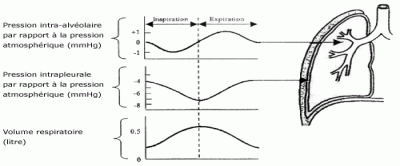
Concentrez-vous sur la première courbe tout en haut. Il s’agit de la différence entre la pression atmosphérique (760 mmHg) et la pression intra-alvéolaire dont nous vous parlions (759 mmHg lors de l’inspiration). Donc lors de l’inspiration cette différence est négative (-1) et l’air entre dans les poumons. Parallèlement à cela la courbe tout en bas montre que le volume augmente pour atteindre environ 0,5 litre en fin d’inspiration : 0,5 litre c’est le volume courant, c’est-à-dire le volume d’air qu’on a à peu près dans les poumons lors d’une inspiration.
Lors d’une expiration
C’est le contraire ! Les muscles inspiratoires (diaphragme et intercostaux externes) vont se relâcher et la cage thoracique va rediminuer de volume. Donc la pression intra-alvéolaire va augmenter et passer de 759 mmHg à 761 mmHg. Cette fois-ci l’air va donc passer des poumons vers le milieu environnant et la différence entre la pression atmosphérique et la pression intra-alvéolaire devient positive (voir la courbe précédente lors de l’expiration). Parallèlement à cela le volume dans les poumons rediminue pour revenir au niveau de base.
Et ce cycle d’inspirations/expirations va donc se répéter tout au long de la vie de l’individu.
Notion de pression partielle d’un gaz
Maintenant nous vous avons parlé d’air en général mais ce qui nous intéresse c’est le dioxygène. Vous savez que l’air est composé d’un mélange de plusieurs gaz dans des proportions différentes, grosso-modo : 21% de dioxygène, 79% de diazote et des traces de dioxyde de carbone et de vapeur d’eau. Les molécules de chaque gaz exercent une certaine pression, c’est-à-dire une force par unité de surface (l’unité étant le Newton par mètre carré de surface = le Pascal). Au niveau de la mer nous pouvons mesurer la pression totale qui résulte de la somme des pressions de ces différents gaz et on trouve une valeur de 760 mmHg. Cela ne vous rappelle rien ? Eh oui, c’est la pression atmosphérique !
En fait chaque gaz de l’air contribue à cette pression totale : par exemple le dioxygène représente 21% des gaz de l’air et ces 21% représentent donc 160 mmHg par rapport à 760 mmHg : 160 mmHg c’est la pression partielle du dioxygène atmosphérique.
Si on prend le diazote qui représente 79% des gaz de l’air on trouve que 79% de 760 mmHg c’est 600 mmHg : 600 mmHg c’est la pression partielle du diazote atmosphérique.
On retombe bien sur 600 mmHg + 160 mmHg = 760 mmHg.
Pour formuler ça de façon plus scientifique nous venons en réalité de vous exposer la loi de Dalton. Cette loi stipule que la pression totale (aussi appelée pression absolue, ici la pression atmosphérique) est égale à la somme des pressions partielles de chaque gaz constituant le mélange gazeux (le mélange étant ici l’air atmosphérique).
Voici un tableau donnant les pressions partielles des différents gaz et leur proportion dans l’atmosphère :
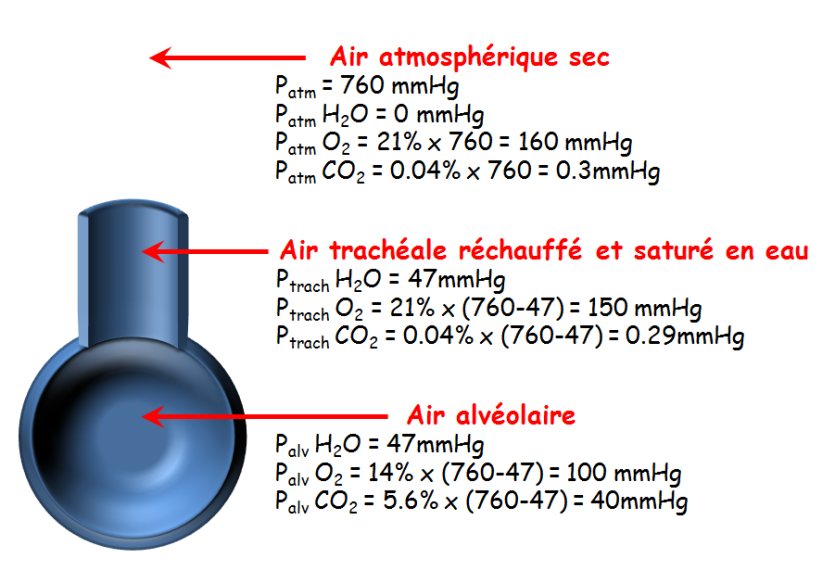
Ce qui va nous intéresser pour la suite c’est la deuxième colonne de ce tableau avec les pressions partielles de ces mêmes gaz mais au niveau des alvéoles pulmonaires cette fois-ci, et non plus de l’atmosphère. Car après tout, ce qui nous intéresse c’est notre organisme. Ce qu’on remarque c’est que les proportions des différents gaz ont changé entre l’air environnant et les alvéoles. Il y a un peu moins de diazote et de dioxygène au profit d’un peu plus de dioxyde de carbone et de vapeur d’eau, qui étaient à l’état de traces dans l’air ambiant. Cela explique donc que les pressions partielles du dioxygène et diazote soient plus faibles entre l’air ambiant et les alvéoles. Par exemple, en prenant le cas du dioxygène, celui-ci ne représente plus que 14% des gaz constituant l’air alvéolaire, sur une pression totale de 760 mmHg cela représente environ 106 mmHg (selon les pourcentages et arrondis on peut arriver à 100 mmHg pour la pression partielle du dioxygène alvéolaire et c’est la valeur que nous prendrons pour la suite du cours). Pour le dioxyde de carbone, celui-ci ne représente plus que 5,2% des gaz constituant l’air alvéolaire, sur une pression totale de 760 mmHg cela représente environ 40 mmHg pour la pression partielle du dioxyde de carbone alvéolaire.
Voyez donc bien ce qu’il s’est passé : la personne inspire, le dioxygène passe dans la trachée, puis les bronches et gagne enfin les alvéoles pulmonaires. Tout au long de ce trajet l’air est humidifié et réchauffé, la vapeur d’eau est donc de plus en plus présente et le dioxyde de carbone est également davantage présent au niveau des alvéoles (car c’est le lieu d’où il vient tout juste, rappelez-vous avec une des images précédentes, le dioxyde de carbone passe du sang vers les alvéoles donc au niveau des alvéoles il est plus présent qu’au niveau du début de l’arbre respiratoire).
Cette valeur de 100 mmHg pour la pression partielle du dioxygène alvéolaire est importante. De manière générale la notion de pression partielle est cruciale pour continuer de comprendre le cours donc si vous n’avez pas trop compris n’hésitez pas à revenir en arrière puis à relire à tête reposée. 
…et de physiologie circulatoire
Nous voulons savoir comment le cyanure diminue l’extraction du dioxygène par les tissus. Nous venons de voir que ce n’est pas en diminuant la production d’ATP puisque le dioxygène peut entrer dans les cellules sans ATP. Nous avons donc étudié la physiologie respiratoire pour acquérir les bases et tenter d’expliquer comment le cyanure diminue l’oxygénation des tissus. Nous n’en sommes qu’à la moitié puisque pour comprendre le phénomène il reste à savoir comment le dioxygène est distribué aux différents tissus une fois qu’il a été inspiré et qu’il se retrouve dans le sang. En étudiant la physiologie circulatoire nous aurons alors sans doute une chance d’expliquer le mode d’action du cyanure sur la diminution d’oxygénation des tissus.
La diffusion du dioxygène depuis les alvéoles vers le sang
Mais première chose il faut savoir comment le dioxygène présent dans les alvéoles va gagner le sang.
Vous connaissez déjà une partie du phénomène (si si nous vous l’assurons  ) : le dioxygène peut passer les membranes des pneumocytes côté alvéolaire et celles des cellules endothéliales côté sang pour gagner le sang et cela se fait par diffusion simple.
) : le dioxygène peut passer les membranes des pneumocytes côté alvéolaire et celles des cellules endothéliales côté sang pour gagner le sang et cela se fait par diffusion simple.
Pour la suite il faut savoir que le corps dispose en réalité de deux types de circulations : une circulation systémique (avec des artères contenant du sang riche en dioxygène et pauvre en dioxyde de carbone - et des veines contenant du sang pauvre en dioxygène et riche en dioxyde de carbone) et une circulation pulmonaire (avec deux artères pulmonaires contenant du sang pauvre en dioxygène et riche en dioxyde de carbone - et quatre veines pulmonaires contenant du sang riche en dioxygène et pauvre en dioxyde de carbone).
Ainsi, au sens strict, les artères ne contiennent pas toujours du sang riche en dioxygène et pauvre en dioxyde de carbone. De la même façon les veines ne contiennent pas toujours du sang pauvre en dioxygène et riche en dioxyde de carbone. C’est vrai pour la circulation systémique mais pas pour la circulation pulmonaire.
Voici une image pour mieux situer ces deux types de circulation dans l’organisme :
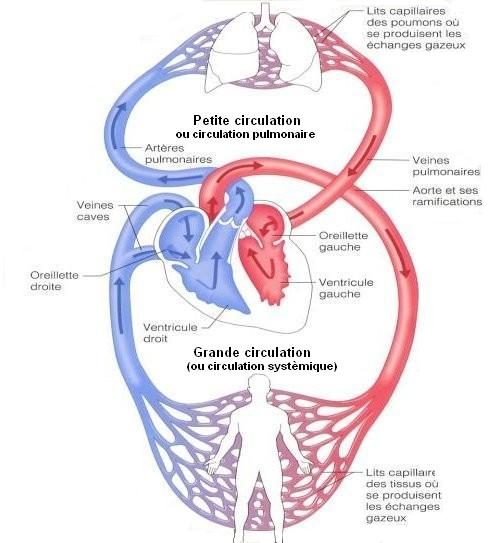
Ce qui va nous intéresser sur ce schéma c’est toujours l’interface air/sang entre les capillaires pulmonaires tout en haut et les alvéoles pulmonaires. Comme déjà dit dans une partie précédente, le sang pauvre en dioxygène en provenance de l’artère pulmonaire (en bleu sur l’image) va être enrichi en dioxygène et se décharger de son dioxyde de carbone : c’est l’hématose. La diffusion d’un gaz se fait toujours de la pression partielle la plus grande vers la pression partielle la plus faible : cela est important puisque nous pouvons prévoir le sens de déplacement des différents gaz.
Pour rappel la pression partielle en dioxygène alvéolaire est de 100 mmHg, dans l’artère pulmonaire la pression partielle en dioxygène n’est que de 40 mmHg. Vous pouvez donc conclure que le dioxygène diffusera des alvéoles vers le sang en provenance de l’artère pulmonaire, cela se fait au niveau des capillaires pulmonaires (lieu des échanges gazeux entre l’alvéole et le sang). Cette diffusion se fait jusqu’à équilibre des pressions partielles : ici jusqu’à ce qu’on ait 100 mmHg dans les alvéoles et dans le sang. Cela explique qu'en sortie des capillaires pulmonaires la pression partielle en dioxygène soit de 100 mmHg dans les veines pulmonaires.
Vous avez donc deux nouvelles données pour la pression partielle du dioxygène : elle est de 100 mmHg dans les veines pulmonaires (et donc dans les artères de la circulation systémique) mais seulement de 40 mmHg dans les deux artères pulmonaires (et donc dans les veines de la circulation systémique). Cela explique que les veines de la circulation systémique renferment du sang pauvre en dioxygène alors que les artères de la circulation systémique renferment du sang riche en dioxygène.
Concernant le dioxyde de carbone rappelez-vous que sa pression partielle vaut 40 mmHg dans les alvéoles. Dans le sang des artères pulmonaires (et donc dans les veines de la circulation systémique) la pression partielle du dioxyde de carbone vaut 45 mmHg. Le dioxyde de carbone diffuse donc des artères pulmonaires (plus précisément des capillaires pulmonaires) vers les alvéoles pour ensuite être expiré. Comme la diffusion se fait jusqu’à équilibre des pressions partielles en dioxyde de carbone, la pression partielle de dioxyde de carbone alvéolaire vaut bien 40 mmHg et la pression partielle de dioxyde de carbone dans les veines pulmonaires (et donc dans les artères de la circulation systémique) vaut donc également 40 mmHg.
Ces valeurs de pressions partielles pour le dioxygène et dioxyde de carbone sont importantes à retenir car elles permettent de prévoir le sens de diffusion des gaz. Vous voyez que vous pouvez les retrouver par la logique en considérant que la diffusion se fait jusqu’à équilibre des pressions partielles. Voici également un schéma qui les résume et les replace dans les deux circulations :
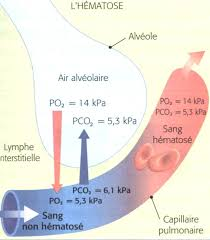
Le transport du dioxygène dans le sang
On commence à toucher au but ! Si le cyanure diminue l’extraction du dioxygène par les tissus alors ce phénomène doit avoir lieu dans le sang. Avant toute chose concentrons-nous sur le transport du dioxygène dans le sang. Vous savez maintenant comment le dioxygène passe des alvéoles vers le sang mais ce que vous ne savez pas c’est le devenir du dioxygène une fois dans le sang et surtout comment il va pouvoir être distribué aux tissus qui en ont besoin.
Il faut savoir quelque chose d’important : le dioxygène peut avoir plusieurs formes de transport dans le sang et précisément deux formes. Il peut soit être libre dans le sang, c’est-à-dire se solubiliser dedans pour ensuite être transporté aux différents organes du corps. Mais le dioxygène est très peu soluble dans le sang (et de manière générale dans l’eau et le sang en contient beaucoup). Il faut aussi savoir que seule la forme dissoute d’un gaz dans le sang contribue à la pression partielle de ce gaz dans le sang. Par exemple lorsque le dioxygène passe des alvéoles vers le sang, les 100 mmHg que vous avez dans le sang sont uniquement dues au dioxygène dissout dans le sang, en clair au dioxygène qui n’est lié à rien. Et justement ça tombe bien parce que le dioxygène peut être lié à quelque chose et précisément à l'hémoglobine.
L’hémoglobine est une protéine à l’intérieur des globules rouges. Quand le dioxygène passe des alvéoles vers le sang il peut :
- soit ne se lier à rien et se solubiliser dans le sang : dans ce cas il contribue à la pression partielle en dioxygène dans les veines pulmonaires ;
- soit il ne veut pas être seul et va se lier à une molécule d’hémoglobine après avoir pénétré dans un globule rouge. Et ça tombe bien car le dioxygène peut traverser librement les membranes des globules rouges pour gagner l’hémoglobine. Cette partie du dioxygène liée à l’hémoglobine ne contribue pas à la pression partielle du dioxygène dans les veines pulmonaires. L’hémoglobine quand elle est liée au dioxygène est appelée oxyhémoglobine. Une molécule d’hémoglobine peut lier 4 molécules de dioxygène.
Voilà donc les deux formes possibles de transport du dioxygène une fois dans le sang.
Nous soulevons donc ici un point important car cela montre bien l’utilité de l’hémoglobine. Elle permet non seulement au dioxygène d’être mieux transporté (car il est peu soluble dans le sang) mais aussi au sang d’être plus enrichi en dioxygène que s’il n’y avait pas d’hémoglobine !
Puisque pour rappel la diffusion du dioxygène depuis les alvéoles vers le sang se fait jusqu’à équilibre des pressions partielles en dioxygène. S’il n’y avait pas d’hémoglobine alors tout le dioxygène ayant gagné le sang contribuerait à la pression partielle et donc l’équilibre se ferait plus vite, donc l’arrêt de la diffusion du dioxygène également.
Or là vous voyez bien que le fait que le dioxygène puisse se lier à l’hémoglobine et donc ne pas contribuer à la pression partielle retarde cet équilibre et donc permet au sang d’avoir davantage de dioxygène (celui lié à l’hémoglobine) en plus d’avoir un meilleur transport du dioxygène.
L’hémoglobine c’est donc l’autoroute pour le dioxygène alors que le sang tout seul c’est une vieille route de campagne sinueuse (même si nous n’avons rien contre les campagnards hein  ).
).
Pour le dioxyde de carbone c’est pareil, il a plusieurs formes de transport dans le sang, pas deux mais trois (jamais deux sans trois dirait-on  ) :
) :
- soit il va être libre dans le sang et contribuer à la pression partielle en dioxyde de carbone dans le sang ;
- soit il va être lié à l’hémoglobine mais pas au même niveau que le dioxygène. Le dioxygène se lie au niveau de l’hème de l’hémoglobine, c’est-à-dire au niveau d’un atome de fer. Le dioxyde de carbone, lui, va se lier au niveau de la partie protéique de l’hémoglobine, aussi appelée la partie globine. Cette partie du dioxyde de carbone liée à l’hémoglobine ne contribue pas à la pression partielle du dioxyde de carbone dans le sang. L’hémoglobine liée au dioxyde de carbone est appelée carbhémoglobine. ;
- soit il va se décomposer en ions (protons) et ions bicarbonates sous l’action d’une enzyme du globule rouge appelée l'anhydrase carbonique. En réalité le passage entre le dioxyde de carbone et ces protons n’est pas direct, voici la réaction précise :
Deux mots concernant cette troisième forme de transport : l’anhydrase carbonique dans le globule rouge permet le passage mais cette réaction peut être spontanée dans le sang, à l’extérieur du globule rouge. Cela explique que lorsque le sang est trop riche en dioxyde de carbone son pH diminue (puisque finalement il y aura plein de protons dans le sang). Retenez également bien les doubles flèches, cela signifie que les réactions sont réversibles et peuvent se faire dans les deux sens, cela aura une importance cruciale pour la suite.
La distribution du dioxygène aux différents tissus
Nous allons maintenant entrer dans le vif du sujet. C’est bien de savoir comment le dioxygène est transporté dans le sang mais pour comprendre comment le cyanure limite la distribution du dioxygène aux tissus il semble nécessaire de savoir comment le dioxygène est distribué aux organes. Déjà il faut savoir que les échanges gazeux entre le sang et les tissus ont lieu dans les capillaires, là le dioxygène est distribué aux organes qui vont consommer ce dioxygène dans la chaîne respiratoire mitochondriale, rappelez-vous du chapitre précédent. Parallèlement du dioxyde de carbone va être rejeté par ces tissus, pour rappel le dioxyde de carbone est produit par les cellules métaboliquement actives durant le cycle de Krebs, comme nous l’avons déjà vu. Le dioxygène au niveau des capillaires va donc devoir diffuser du sang vers les tissus. Et ça n’est pas un problème, si nous vous remettons l’image précédente :

Vous voyez, tout en bas de l’image, que la pression partielle du dioxygène dans les tissus est toujours inférieure à 40 mmHg. Dans les artères systémiques (et donc à l’arrivée des capillaires) vous savez maintenant que la pression partielle en dioxygène est de 100 mmHg. Hop hop hop, réflexe, sens de déplacement du dioxygène ? Eh oui, bravo, du sang vers les tissus, ce n’est pas magique tout ça ? 
Pareil, vous voyez que la pression partielle du dioxyde de carbone dans les tissus est toujours supérieure à 45 mmHg. Dans les artères systémiques vous savez que la pression partielle en dioxyde de carbone est de 40 mmHg et donc le dioxyde de carbone va diffuser des tissus vers le sang, jusqu’à équilibre des pressions partielles en dioxyde de carbone.
Cela explique alors la diminution de pression partielle du dioxygène entre les artères systémiques et les veines systémiques, on passe de 100 mmHg à 40 mmHg car le dioxygène est distribué aux tissus. Au contraire la pression partielle de dioxyde de carbone augmente entre les artères systémiques et les veines systémiques, on passe de 40 mmHg à 45 mmHg car le dioxyde de carbone est rejeté par les tissus métaboliquement actifs.
Eh bien voilà c’est fini, nous savons comment le dioxygène est distribué aux tissus et le dioxyde de carbone rejeté dans le sang…
…
…
…
…
…
Oui mais non. On aurait pu s’arrêter là, ça aurait fait une belle histoire mais il y a toujours un MAIS. 
Rappelez-vous que nous vous avions dit que le dioxygène avait deux formes de transport. Il pouvait être libre dans le sang et nous venons de voir que ce dioxygène libre est distribué aux tissus par diffusion simple du sang vers les tissus selon le gradient de pression partielle. Tout ce qu’il y a de plus simple (c’est le cas de le dire), vous commencez à devenir des pros maintenant j’espère. 
Mais il pouvait aussi et surtout être lié à l’hémoglobine. Et nous n’avons pas encore vu comment le dioxygène lié à l’hémoglobine pouvait justement s’en détacher pour être distribué aux tissus.
Il faut avoir en tête que le dioxygène n’oxyde pas l’hémoglobine lorsqu’il y est lié mais il s’agit d’une réaction d’oxygénation, ce qui est bien différent au niveau fonctionnel. En effet l’oxydation entrainerait une nouvelle forme d’hémoglobine appelée méthémoglobine. Cette forme d’hémoglobine ne peut plus se détacher de son dioxygène et n’est donc pas utile physiologiquement, c’est même dangereux d’en avoir trop car les tissus ne pourront alors plus extraire le dioxygène depuis cette forme de l’hémoglobine. De manière physiologique nous avons toujours un tout petit peu de méthémoglobine, ce n’est pas dangereux et une enzyme appelée la méthémoglobine réductase permet de reformer l’hémoglobine depuis la méthémoglobine. Donc nous disions qu’il s’agit d’une réaction d’oxygénation pour produire une forme d’hémoglobine dont nous avons déjà parlé : l’oxyhémoglobine. Cette forme, contrairement à la méthémoglobine, pourra se séparer de son dioxygène pour le donner aux tissus au niveau des capillaires sanguins.
Vous voyez le tableau qui se dessine ? Et si justement le cyanure favorisait la formation de méthémoglobine pour empêcher le dioxygène d’être distribué aux tissus dans les capillaires ? Personnellement nous trouvons l’hypothèse séduisante et ce sera donc notre deuxième hypothèse. J’espère que cette fois-ci nous n’allons pas nous planter en beauté comme la première fois. 
Mais avant tout étudions ce qu’il se passe dans un cas normal. Nous reviendrons sur notre hypothèse à la fin de ce cours.
Le dioxygène arrive au niveau des veines pulmonaires, là sa pression partielle vaut 100 mmHg. Une partie est dissoute dans le sang, une autre va aller sur l’hémoglobine au niveau du fer ferreux (ion ) pour donner l’oxyhémoglobine. Nous vous avions déjà dit que l’hémoglobine peut fixer 4 molécules de dioxygène mais ce que nous ne vous avions pas dit c’est que plus l’hémoglobine fixe de molécules de dioxygène plus elle aura d’affinité pour fixer d’autres molécules de dioxygène. Par exemple une molécule d’hémoglobine ayant déjà fixé 2 molécules de dioxygène aura plus de facilité à en fixer une 3ème. Par contre une molécule d’hémoglobine ayant fixé 1 seule molécule de dioxygène aura plus de mal à en fixer une 2ème. On pourrait résumer ce processus par la phrase suivante : "pour l’hémoglobine l’appétit vient en mangeant." Plus elle aura fixé de molécules de dioxygène plus il lui sera facile d’en fixer une autre. Autrement dit la fixation d’une molécule de dioxygène sur un site de l’hémoglobine (au niveau de l’hème sur un fer ferreux) modifie l’affinité de l’hémoglobine pour d’autres molécules de dioxygène et ici cette modification est positive car l’affinité sera augmentée : on dit que le dioxygène est un effecteur homotrope positif et on parle aussi de coopérativité positive.
Homotrope car les molécules qui se fixent sur l’hémoglobine et celles dont l’affinité vis-à-vis de l’hémoglobine est modifiée (suite à cette liaison) sont les mêmes : dans notre cas c’est le dioxygène.
Positif car la liaison du dioxygène au niveau d’un fer ferreux augmente l’affinité de l’hémoglobine pour d’autres molécules de dioxygène.
Et enfin on parle de coopérativité positive car il y a une sorte de coopération entre les molécules de dioxygène, comme nous venons de le dire la fixation d’une molécule de dioxygène sur l’hémoglobine augmente l’affinité de l’hémoglobine pour les molécules de dioxygène suivantes.
Cette notion est très importante pour la suite. Ce que nous venons de vous présenter c’est en fait la notion d'allostérie. C’est-à-dire que la fixation d’une molécule en un site d’une protéine modifie les conditions de fixation d’une autre molécule en un autre site distant de cette même protéine. De manière plus générale la notion s’applique aux enzymes dites allostériques qui possèdent, en plus du site actif, un site régulateur où vient se fixer l’effecteur, cela modifiera les conditions de fixation de l’autre molécule au niveau du site actif (en augmentant ou diminuant l’affinité).
Toutes les enzymes de l’organisme ne sont pas allostériques, les autres sont dites Michaeliennes.
Nous n’allons pas nous attarder sur cette notion d’enzymes Michaeliennes ni même d’enzymes allostériques puisque ce qui nous intéresse c’est l’hémoglobine, qui n’est pas une enzyme mais une protéine de transport. Notez cependant bien que le fonctionnement reste plus ou moins le même qu’une enzyme allostérique et ce sont les notions en rapport avec les conditions de fixation du dioxygène sur l’hémoglobine que nous venons de vous présenter qui sont importantes à retenir. L’image qui suit résume un peu ce qui vient d’être dit :
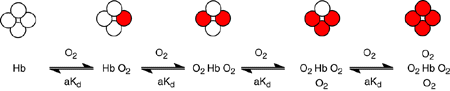
Un rond blanc correspond à un site de fixation du dioxygène, c’est-à-dire l’hème contenant le fer ferreux. Il y a quatre molécules de dioxygène pouvant être fixées par molécule d’hémoglobine donc quatre ronds. Lorsqu’un rond fixe une molécule de dioxygène vous pouvez voir que la fixation est réversible car il y a une double flèche. Quand l’hémoglobine a fixé une molécule de dioxygène elle peut relâcher la molécule qu’elle vient de fixer pour retourner à un état de base sans aucune molécule de dioxygène liée. Et plus elle aura fixé de molécules de dioxygène plus elle aura tendance à en fixer jusqu’à ne plus pouvoir en fixer, à ce moment on dit que l’hémoglobine sera saturée.
Tout ce que nous venons de dire nous amène à penser à une chose : le niveau de saturation de l’hémoglobine devrait alors dépendre du taux de dioxygène disponible dans son environnement proche.
Et nous avons une bonne nouvelle pour vous, c’est bien le cas !  Vous allez comprendre pourquoi maintenant, voici une jolie courbe :
Vous allez comprendre pourquoi maintenant, voici une jolie courbe :
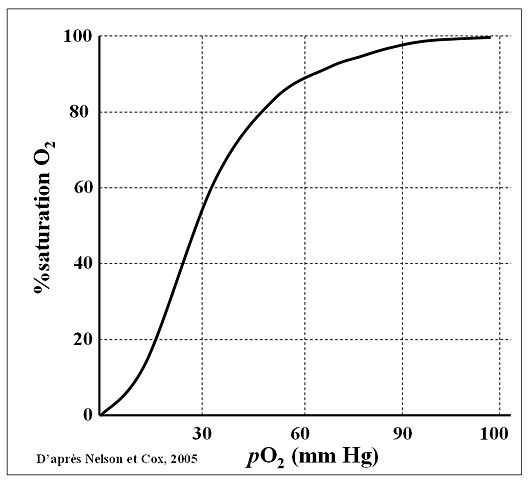
Cette courbe c’est THE courbe à retenir !
On l’appelle courbe de Barcroft, courbe de dissociation de l’oxyhémoglobine ou même courbe de saturation de l’hémoglobine en fonction de la pression partielle de dioxygène (ça en fait des noms  ).
Il y a souvent des confusions qui peuvent être faites à partir de cette courbe ou bien des sur-interprétations, mon but ça va être de vous éviter tout cela. Je le dis car je suis passé par là, j’ai moi-même fait beaucoup d’erreurs au départ concernant cette courbe et je connais aussi pas mal de gens en ayant fait, que ce soit dans mon entourage ou sur internet (bon ok j’arrête de vous raconter ma vie
).
Il y a souvent des confusions qui peuvent être faites à partir de cette courbe ou bien des sur-interprétations, mon but ça va être de vous éviter tout cela. Je le dis car je suis passé par là, j’ai moi-même fait beaucoup d’erreurs au départ concernant cette courbe et je connais aussi pas mal de gens en ayant fait, que ce soit dans mon entourage ou sur internet (bon ok j’arrête de vous raconter ma vie  ).
Mais si vous suivez attentivement tout devrait bien se passer.
).
Mais si vous suivez attentivement tout devrait bien se passer.
Première chose à savoir : on parle de la pression partielle de dioxygène au niveau sanguin. Donc la pression partielle en abscisse de 100 mmHg est par exemple celle retrouvée au niveau des veines pulmonaires et artères systémiques. Celle de 40 mmHg est celle retrouvée au niveau des capillaires systémiques (en sortie des capillaires), veines systémiques et artères pulmonaires.
Deuxième chose à savoir : on lit cette courbe de droite à gauche. Eh oui, cela peut vous sembler bizarre mais c’est comme ça. Pourquoi de droite à gauche ? Car il est intuitif de partir de la pression partielle en dioxygène rencontrée au niveau des veines pulmonaires, juste en sortie des poumons, là où le sang vient de se recharger en dioxygène. Puis ensuite on parcourt l’arbre circulatoire jusqu’aux capillaires où le dioxygène diffuse vers les tissus, ce qui abaisse la pression partielle en dioxygène à 40 mmHg. Ensuite on revient aux poumons via les veines et artères pulmonaires et là la courbe peut se lire de gauche à droite (cheminement inverse avec la pression partielle en dioxygène qui repasse de 40 mmHg à 100 mmHg).
Troisième chose à savoir : la saturation indiquée en ordonnée est la saturation de l’hémoglobine totale donc au niveau de toutes les molécules d’hémoglobine de tous les globules rouges du corps. 100% de saturation indique qu’absolument toutes les molécules d’hémoglobine de tous les globules rouges ont fixé des molécules de dioxygène et que les quatre sites de chaque molécule d’hémoglobine sont occupés. 0% indique qu’aucune molécule d’hémoglobine n’a fixé ne serait-ce qu’une seule molécule de dioxygène (ce qui n’arrive jamais sinon c’est que vous êtes mort).
Dernière chose à savoir : la forme de la courbe est une sigmoïde en "S" et non une droite. Cela a un rapport avec le comportement allostérique de l’hémoglobine dont nous vous avions parlé précédemment et justement nous allons tout de suite nous étendre sur ce sujet.
Rappelez-vous, quelques lignes au-dessus nous vous avions dit que le degré de saturation de l’hémoglobine pourrait bien dépendre du taux de dioxygène environnant, plus exactement de la pression partielle en dioxygène. On voit avec cette courbe que c’est bien le cas puisque moins il y a de dioxygène (la pression partielle en dioxygène diminue) moins l’hémoglobine est saturée donc plus elle relâche le dioxygène qu’elle avait fixé. Au niveau des capillaires pulmonaires, là où il y a beaucoup de dioxygène qui vient d’être inspiré, la pression partielle en dioxygène vaut 100 mmHg et l’hémoglobine est saturée à près de 95%. En effet, à cet endroit là de l’arbre circulatoire, imaginons qu’une molécule de dioxygène se détache d’un site d’une molécule d’hémoglobine, c’est tout à fait possible puisque pour rappel la liaison est réversible, alors cette molécule de dioxygène serait immédiatement remplacée par une autre molécule de dioxygène de l’environnement proche car il y a beaucoup de dioxygène disponible dans cet environnement. Finalement l’hémoglobine restera très saturée en dioxygène.
Maintenant descendons plus en profondeur dans l’arbre circulatoire. Nous sommes au niveau des capillaires systémiques des tissus, là le dioxygène passe des capillaires vers les tissus car ils consomment du dioxygène. Cela abaisse la pression partielle de dioxygène à 40 mmHg. À cet endroit là si une molécule de dioxygène se détache d’un site d’une molécule d’hémoglobine alors le remplacement sera plus difficile puisque le dioxygène a diffusé vers les tissus et il y en a moins dans le sang. L’hémoglobine n’aura pas tous ses sites liant du dioxygène, par exemple beaucoup de molécules d’hémoglobine n’auront que deux des quatre sites ayant fixé du dioxygène. Au niveau des capillaires systémiques on a une saturation typique d’environ 70%.
Enfin imaginons, toujours au niveau des capillaires, que des muscles travaillent vraiment beaucoup, par exemple en plein effort. Le dioxygène sera encore plus consommé et diffusera davantage vers ces muscles et donc la pression partielle en dioxygène sera encore plus abaissée, elle ne vaudra plus 40 mmHg mais quelque chose comme 20 mmHg. Si une molécule de dioxygène se détache d’un site d’une molécule d’hémoglobine alors le remplacement sera cette fois-ci vraiment difficile puisqu’il n’y aura que peu de dioxygène dans le sang de ces capillaires. Beaucoup de molécules d’hémoglobine auront un seul site ayant fixé une molécule de dioxygène, sur les quatre pourtant disponibles. Le fait qu’un seul site soit occupé par une molécule de dioxygène participe également à maintenir l’hémoglobine dans cet état de faible saturation car rappelez-vous que selon le principe d’allostérie par coopérativité positive plus l’hémoglobine fixe de molécules de dioxygène plus il est facile d’en fixer une autre. Avec une seule molécule fixée ce sera donc plus difficile d’en fixer une deuxième. Dans ce cas on retrouve une saturation d’environ 30% et tant mieux car les muscles ont besoin de dioxygène en cas d’effort intense, donc le fait d’en avoir moins sur l’hémoglobine signifie qu’il est parti vers ces muscles.
Partons maintenant un peu en altitude. Vous savez qu’en altitude il y a moins de dioxygène disponible dans l’air et que la pression atmosphérique est plus basse. Cela signifie qu’au niveau des alvéoles pulmonaires la pression partielle en dioxygène est également plus faible, typiquement à 2400 m d’altitude on retrouve une pression partielle en dioxygène alvéolaire de 60 mmHg et non plus de 100 mmHg. La diffusion du dioxygène depuis les alvéoles vers le sang se fera donc jusqu’à atteindre un équilibre de 60 mmHg pour la pression partielle en dioxygène dans les capillaires pulmonaires. Au niveau de la courbe ci-dessus si vous lisez le degré de saturation correspondant à 60 mmHg vous voyez que l’hémoglobine est toujours très saturée, environ 90%. Pourtant on a diminué la pression partielle de 40% en passant de 100 mmHg à 60 mmHg ! Autrement dit il y a une phase de plateau pour cette courbe.
C’est-à-dire qu’à 60 mmHg de pression partielle en dioxygène : si une molécule de dioxygène se détache d’un site d’une molécule d’hémoglobine alors le remplacement de la molécule de dioxygène sera plus difficile car il y a moins de dioxygène dans le sang mais cependant moins difficile qu’à 40 mmHg. En effet à 60 mmHg l’hémoglobine aura relâché des molécules de dioxygène mais pas suffisamment pour qu’elle ait du mal à en refixer d’autres (et donc remplacer le dioxygène qui a été relâché) car rappelez-vous, selon le principe d’allostérie par coopérativité positive, moins l’hémoglobine aura lié de molécules de dioxygène plus la fixation d’autres molécules de dioxygène sera difficile.
Cela explique qu’à 40 mmHg la saturation diminue de manière brutale avec une forte pente pour cette courbe. À 40 mmHg le sang est moins enrichi en dioxygène dissout, l’hémoglobine relâche des molécules de dioxygène et le remplacement de ces molécules sera donc encore plus difficile qu’à 60 mmHg. L’hémoglobine est encore moins saturée qu’à 60 mmHg et donc l’hémoglobine a plus de mal à refixer d’autres molécules de dioxygène.
Ainsi en passant de 100 mmHg à 60 mmHg on diminue moins la saturation de l’hémoglobine que si on passe de 60 mmHg à 40 mmHg et pourtant la différence entre 100 mmHg et 60 mmHg est plus grande que celle entre 60 mmHg et 40 mmHg. Cela s’explique par le comportement allostérique de cette protéine et explique la forme sigmoïde de cette courbe. Moins il y a de dioxygène lié à l’hémoglobine plus il est difficile pour l’hémoglobine de lier d’autres molécules de dioxygène. La liaison du dioxygène à l’hémoglobine s’observe lorsque l’on remonte l’arbre circulatoire (depuis les capillaires systémiques jusqu’aux capillaires pulmonaires) quand la pression partielle en dioxygène réaugmente alors que la dissociation du dioxygène de l’hémoglobine s’observe lorsque l’on redescend l’arbre circulatoire (depuis les capillaires pulmonaires jusqu’aux capillaires systémiques) quand la pression partielle en dioxygène rediminue. Cela explique le nom de cette courbe : dissociation de l’oxyhémoglobine.
En clair : il n’est pas possible de prédire le degré de saturation de l’hémoglobine pour une pression partielle en dioxygène donnée sur la base d’un produit en croix, la situation n’est pas linéaire, il faut bien comprendre ceci.
Maintenant pourquoi avoir parlé de 60 mmHg ? Car cela montre bien l’utilité physiologique du plateau de cette courbe. En altitude nous avons donc 60 mmHg pour la pression partielle du dioxygène des capillaires pulmonaires et une saturation de l’hémoglobine de 90%. Donc les tissus auront toujours assez de dioxygène, ils en auront un peu moins (on passe de 100 mmHg à 60 mmHg donc un peu moins de dioxygène dissout dans le sang et également 5% de saturation de l’hémoglobine en moins) mais ce n’est pas dramatique. C’est donc une sorte de sécurité pour l’organisme, aller en altitude moyenne ne devrait pas vous tuer. 
Jusqu’ici nous vous avions parlé du dioxygène qui pouvait être relâché de la molécule d’hémoglobine seul, c’est-à-dire sans l’aide de facteurs externes. En vérité il existe un certain nombre de facteurs pouvant aussi faciliter le relargage du dioxygène de l’hémoglobine, parmi eux : le dioxyde de carbone, les protons la température élevée et une molécule appelée le 2,3-bisphosphoglycérate (abrégée 2,3-BPG).
Cela devrait vous rappeler quelque chose, nous vous avions précédemment parlé d’allostérie en disant que des molécules pouvaient se lier à un site d’une protéine pour modifier l’affinité d’une autre molécule vis-à-vis de cette même protéine. Eh bien nous sommes pile dans ce cas ! Ici nous avons bien des molécules capables de se fixer sur l’hémoglobine pour favoriser le relargage du dioxygène, ainsi nous dirons que le dioxyde de carbone, les protons, la haute température et le 2,3-BPG constituent des effecteurs hétérotropes négatifs, du point de vue allostérique.
Hétérotrope car les molécules qui se fixent sur l’hémoglobine et celles dont l’affinité vis-à-vis de l’hémoglobine est modifiée (suite à cette liaison) ne sont PAS les mêmes : dans notre cas l’affinité est modifiée pour le dioxygène et les molécules qui se fixent sur l’hémoglobine sont le dioxyde de carbone et le 2,3-BPG. Les protons et la haute température ne sont pas des molécules mais peuvent être classées dans ces effecteurs hétérotropes négatifs.
Négatif car la liaison de ces molécules/ions (ou la haute température) diminue l’affinité de l’hémoglobine pour d’autres molécules de dioxygène.
Tout cela devient logique et pertinent physiologiquement :
-
En effet au niveau des capillaires systémiques les tissus travaillent et relâchent donc du dioxyde de carbone, ce dioxyde de carbone va pouvoir se fixer au niveau de l’hémoglobine (une des trois formes de transport du dioxyde de carbone énoncées précédemment) pour favoriser le relargage du dioxygène, lui-même pourra ensuite diffuser vers ces tissus qui en ont besoin.
-
S’il y a plus de dioxyde de carbone relâché alors l’intérieur du globule rouge sera enrichi en protons. En effet selon la réaction présentée plus tôt dans ce cours (une des trois formes de transport du dioxyde de carbone dans le sang) on a pour rappel : L’anhydrase carbonique à l’intérieur du globule rouge permettra la formation de protons. Ces protons permettront de relâcher plus de dioxygène par l’hémoglobine ;
-
Lors d’un effort ou en cas de fièvre la température au niveau des capillaires systémiques est également localement augmentée. Donc là encore le dioxygène sera relâché de l’hémoglobine pour être distribué aux tissus qui en ont davantage besoin en cas d’effort ou de fièvre ;
-
Le 2,3-BPG, quant à lui, est aussi surproduit en cas d’effort et donc va permettre une plus grande libération de dioxygène depuis l’hémoglobine, dioxygène qui pourra là aussi diffuser vers les tissus.
Ainsi vous comprenez bien que la courbe précédente ne peut pas s’expliquer uniquement par la dissociation du dioxygène tout seul, il faut aussi tenir compte de la libération constante de dioxyde de carbone par les tissus qui va permettre aussi de libérer le dioxygène depuis l’hémoglobine. Donc pour cette courbe de base il faut prendre en compte la dissociation du dioxygène seul depuis l’hémoglobine mais aussi la dissociation du dioxygène facilitée par le dioxyde de carbone et du coup par les protons qui résultent de la réaction ci-dessus. L’ensemble de ces phénomènes permet d’expliquer la saturation de l’hémoglobine observée pour une pression partielle de dioxygène donnée.
Maintenant ce qu’il va falloir comprendre c’est que cette courbe de base correspond à une situation qualifiée de "normale" : la température est de 37°C, le 2,3-BPG n’est pas présent et le dioxyde de carbone (donc les protons et le pH résultant) est libéré en quantité "normale" par les tissus au niveau des capillaires systémiques.
Mais que se passe-t-il si ces paramètres sont modifiés ? Eh bien pour une pression partielle de dioxygène donnée, par exemple 40 mmHg au niveau des capillaires systémiques, nous aurons soit une plus grande désaturation de l’hémoglobine (température augmentée, plus de 2,3-BPG, plus de dioxyde de carbone, plus de protons, pH plus petit = finalement décalage de la courbe de Barcroft vers la droite) soit une moins grande désaturation de l’hémoglobine (température abaissée, moins de dioxyde de carbone, moins de protons, pH plus élevé = finalement décalage de la courbe de Barcroft vers la gauche).
C’est ce qu’on voit sur l’image suivante :
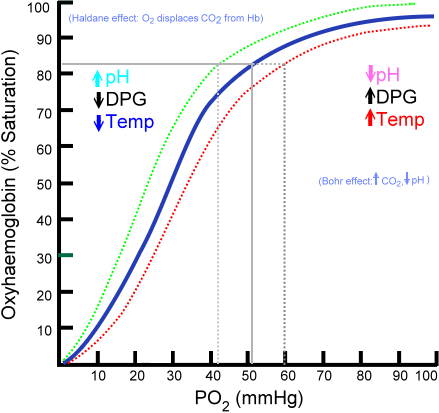
Sur cette image vous voyez également deux noms étranges en anglais : l'effet Bohr et l'effet Haldane. En vérité nous venons de vous parler de ces notions mais sans mettre de nom dessus.
-
Dans l’effet Bohr le dioxyde de carbone et les protons permettent de dissocier de l’hémoglobine le dioxygène. L’effet Bohr est donc un effet allostérique avec comme effecteurs hétérotropes négatifs le dioxyde de carbone et les protons. Cet effet a donc lieu au niveau des capillaires systémiques, là où beaucoup de dioxyde de carbone (et donc de protons) est rejeté par les tissus métaboliquement actifs ;
-
L’effet Haldane, quant à lui, c’est l’inverse. Dans cet effet le dioxygène permet de dissocier de l’hémoglobine le dioxyde de carbone et les protons. Cet effet a donc lieu au niveau des capillaires pulmonaires, là où beaucoup de dioxygène est disponible. Lorsque le dioxyde de carbone est dissocié de l’hémoglobine il est expiré et passe vers les alvéoles selon le gradient de pression partielle en dioxyde de carbone (pour rappel 45 mmHg en début de capillaires pulmonaires et 40 mmHg dans les alvéoles). Lorsque les protons sont dissociés de l’hémoglobine ils peuvent reformer du dioxyde de carbone. En effet rappelez-vous que la réaction catalysée par l’anhydrase carbonique du globule rouge est réversible et peut donc se faire dans les deux sens : Le dioxyde de carbone ainsi reformé quittera le globule rouge et sera expiré après avoir diffusé dans les alvéoles.
Lorsque la molécule d’hémoglobine a beaucoup d’affinité pour le dioxygène (ce qu’il se passe au niveau des capillaires pulmonaires) on dit que la conformation R ("R" pour Relâchée) de l’hémoglobine est favorisée. Au contraire lorsque la molécule d’hémoglobine est dans une conformation ayant peu d’affinité pour le dioxygène (ce qu’il se passe au niveau des capillaires systémiques) on dit que la conformation T ("T" pour Tendue) de l’hémoglobine est favorisée. Cette conformation "T" est due à une modification de la structure tridimensionnelle de l’hémoglobine, cette modification de la structure est permise par l’action des effecteurs hétérotropes négatifs : dioxyde de carbone, 2,3-BPG, haute température et protons. L’effet Bohr, dans lequel le dioxyde de carbone et les protons permettent de dissocier le dioxygène de l’hémoglobine, agit donc en favorisant la conformation T de l’hémoglobine.
Désormais il va falloir savoir comment, au niveau moléculaire, ces différents effecteurs hétérotropes négatifs permettent de dissocier le dioxygène de son hémoglobine.
-
Concernant l’augmentation de température c’est assez simple. Quand la température augmente le degré d’agitation moléculaire augmente, cela permet de chasser le dioxygène de la molécule d’hémoglobine ;
-
Concernant le dioxyde de carbone, nous vous avions dit plus tôt dans le cours que celui-ci se fixait au niveau de la partie protéique de l’hémoglobine appelée la globine. Cette fixation entraîne donc une modification de la structure tridimensionnelle de l’hémoglobine qui passe de la conformation R à T : le dioxygène se dissocie de l’hémoglobine (effet Bohr) ;
-
Concernant les protons, ceux-ci peuvent également se lier à la partie protéique de l’hémoglobine et modifier le pH autour de l’hémoglobine. Cela va permettre de ioniser certains acides aminés de l’hémoglobine et va finalement changer là aussi la structure tridimensionnelle de l’hémoglobine qui passera de la conformation R à T : le dioxygène se dissociera de l’hémoglobine (effet Bohr) ;
-
Concernant le 2,3-BPG, celui-ci se fixe au niveau de la cavité centrale délimitée par la molécule d’hémoglobine. Cela change aussi la conformation de l’hémoglobine et permet de dissocier le dioxygène de son hémoglobine.
Revenons maintenant sur notre hypothèse. Nous avions dit que le cyanure pouvait empêcher la libération du dioxygène depuis l’hémoglobine en favorisant la formation de méthémoglobine, qui pour rappel est une forme d’hémoglobine oxydée (ion ferrique au niveau de l’hème au lieu de l’ion ferreux ) ne pouvant plus se détacher de son dioxygène (liaison irréversible), ce qui est donc dangereux pour l’organisme puisque le dioxygène ne peut plus être donné aux tissus.
Vous pensez bien que si nous vous avons raconté tout une histoire sur l’allostérie c’est qu’il y a une bonne raison, sinon on pouvait plier l’histoire depuis notre hypothèse sur la méthémoglobine. 
Et en effet : cette hypothèse est fausse. Le cyanure empêche bien la libération du dioxygène depuis l’hémoglobine mais pas en favorisant la formation de méthémoglobine.
En réalité le cyanure se fixe sur l’ion ferreux au niveau de l’hème de l’hémoglobine :
- Soit l’hème avait déjà fixé une molécule de dioxygène alors celle-ci ne pourra plus être libérée pour diffuser vers les tissus, au niveau des capillaires systémiques.
C’est-à-dire que le dioxyde de carbone, les protons, la haute température, le 2,3-BPG,
Supermann’y pourront rien, le dioxygène restera collé à son hème ! Et c’est pareil pour ce qui est de la dissociation seule du dioxygène (c’est-à-dire sans facteurs externes), le dioxygène ne pourra plus quitter la molécule d’hémoglobine.
Cela explique qu'en présence de cyanure la courbe de Barcroft soit décalée vers la gauche : pour une pression partielle en dioxygène donnée (celle de 40 mmHg dans les capillaires systémiques) la saturation de l’hémoglobine est augmentée, donc elle n’a pas fait son boulot, elle a encore trop de dioxygène qui est resté sur elle et les tissus n’en ont pas (ou plutôt en ont moins).
- Soit le cyanure peut aussi se lier à un hème n’ayant pas encore fixé de molécule de dioxygène et dans ce cas cette fixation interdit toute fixation de dioxygène sur l’hème concerné. La fixation du cyanure à l’hémoglobine donne une molécule appelée cyanhémoglobine. Donc dans ce cas le dioxygène ne peut même pas se fixer à l’hémoglobine. Cela signifie aussi que la saturation de l’hémoglobine, à 100 mmHg de pression partielle en dioxygène (au niveau des capillaires pulmonaires), sera nettement diminuée. Rappelez-vous du plateau sur la courbe de Barcroft, si cette saturation est abaissée de 95% (cas "normal") à 90% en présence de cyanure, ce n’est pas très grave, ce sera comparable à une situation à 2400 m d’altitude. Dans le cas du cyanure la diminution de saturation est due au fait que le dioxygène ne peut plus se lier à l’hémoglobine, dans le cas de la moyenne altitude c’est dû au fait que la pression partielle en dioxygène dans les capillaires pulmonaires est diminuée (60 mmHg au lieu de 100 mmHg). Mais maintenant imaginez que la saturation soit diminuée plus gravement en présence d’une plus grande quantité de cyanure, on passerait de 95% à 40%. Dans ce cas l’hémoglobine serait déjà désaturée (ou plutôt n’aurait jamais été saturée de manière satisfaisante au niveau des capillaires pulmonaires) avant même d’arriver au niveau des capillaires systémiques ! Autrement dit elle ne fournirait pratiquement pas de dioxygène aux tissus et ça c’est déjà beaucoup plus grave !
Mais rappelez-vous du chapitre précédent : en présence de cyanure, que le dioxygène soit fourni ou non aux tissus il ne pourra de toute façon pas être utilisé dans la chaine respiratoire mitochondriale puisque le cyanure bloque aussi le complexe IV de cette chaine (en se fixant là encore sur l’ion ferrique de ce complexe).
Ainsi les effets que nous avons observés jusqu’ici concernant le cyanure tiennent sur une seule chose : la fixation du cyanure sur les ions de l’hémoglobine ou du complexe IV de la chaine respiratoire mitochondriale.
Il y a quand même un petit lien à faire avec la méthémoglobine donc notre précédente hypothèse n’est pas totalement inutile. 
En effet un antidote possible pour le cyanure consiste à oxyder l’hémoglobine en méthémoglobine. Cela fournit donc un site de fixation alternatif au cyanure car la méthémoglobine contient l’ion ferrique . Le principe est donc d’éviter que le cyanure se fixe trop à ce qui est physiologiquement vital (c’est-à-dire le complexe IV de la chaine respiratoire mitochondriale) en lui disant de se fixer à autre chose, ici l’ion ferrique de la méthémoglobine. C’est un peu un leurre biologique.
On oxyde l’hémoglobine en méthémoglobine à l’aide de nitrites comme les nitrites d’alkyle.
Cependant si vous avez bien suivi jusqu’ici (et j’espère que c’est le cas  ) cet antidote n’est pas sans effet néfaste car la méthémoglobine ne peut pas se dissocier de son dioxygène.
Donc si on transforme trop d’hémoglobine en méthémoglobine on risque de faire l’effet inverse souhaité et de tuer la personne en reproduisant l’effet du cyanure sur le décalage de la courbe de Barcroft vers la gauche mais cette fois-ci sur une plus grande proportion d’hémoglobine.
) cet antidote n’est pas sans effet néfaste car la méthémoglobine ne peut pas se dissocier de son dioxygène.
Donc si on transforme trop d’hémoglobine en méthémoglobine on risque de faire l’effet inverse souhaité et de tuer la personne en reproduisant l’effet du cyanure sur le décalage de la courbe de Barcroft vers la gauche mais cette fois-ci sur une plus grande proportion d’hémoglobine.
Ce chapitre est désormais terminé nous espérons que vous comprenez maintenant mieux comment le cyanure agit sur l’organisme.
Dans le dernier chapitre de cette partie nous vous proposons un grand exercice pour tester les connaissances acquises, c’est assez important pour deux choses. Premièrement cela vous permettra de tester vos connaissances, vous rappeler de ce qui a été dit (répéter est important). Deuxièmement car nous n’allons pas vous faire répéter le cours comme il a été déroulé ici, nous essayons de vous proposer des choses en rapport avec ce qui a été dit mais apportant une vision différente des notions abordées. Nous pensons vraiment que présenter les mêmes choses dans un contexte légèrement différent peut améliorer la compréhension des phénomènes. 
Concernant ce chapitre voici l’essentiel de ce qu’il faut retenir :
L’essentiel : lors d’une inspiration le dioxygène arrive au niveau des alvéoles pulmonaires où il devient sous-représenté par rapport aux autres gaz de l’alvéole (14% contre 21% dans l’air qui nous entoure). Le dioxygène diffuse des alvéoles vers le sang des capillaires pulmonaires selon le gradient de pression partielle en dioxygène. Cela permet de saturer l’hémoglobine des globules rouges à ce niveau et une faible partie du dioxygène se dissout aussi dans le sang. Dans les capillaires au niveau des tissus, le dioxygène diffuse du sang vers les tissus selon le gradient de pression partielle et une partie de l’hémoglobine libère aussi son dioxygène. L’hémoglobine partiellement désaturée en dioxygène ainsi que le sang appauvri en dioxygène dissout reviennent au niveau des capillaires pulmonaires pour récupérer du dioxygène. Le cycle recommence indéfiniment. Le cyanure se lie au fer ferreux de l’hémoglobine et cela empêche l’hémoglobine de libérer le dioxygène qu’elle a fixé, les tissus ont donc moins de dioxygène pour fonctionner. Même si le dioxygène pouvait être libéré aux tissus il ne pourrait être utilisé par ceux-ci. En effet le cyanure se lie aussi au fer ferrique du complexe IV de la chaîne respiratoire mitochondriale, empêchant toute utilisation du dioxygène par les mitochondries de ces tissus.