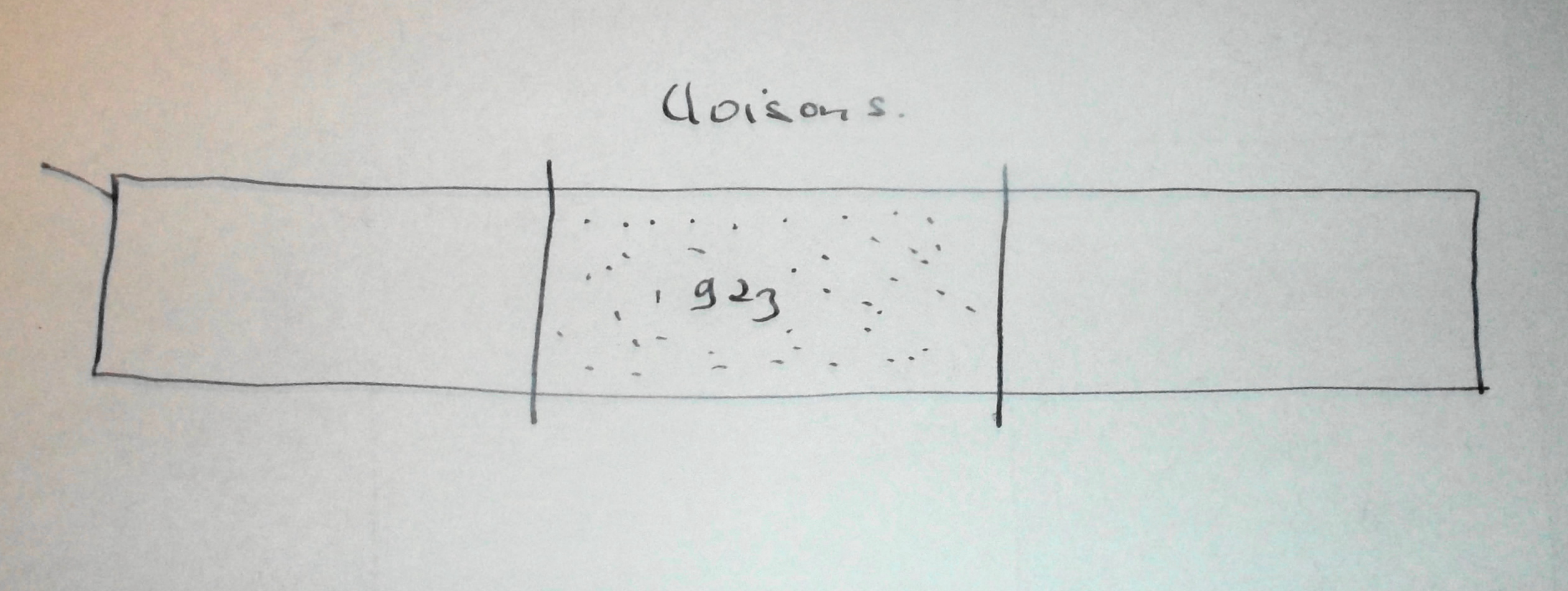
J’ai pas tout compris.
De ce que je comprends, dans les cas présentés dans ton premier message, une force va apparaitre. Si on tente d’estimer cette force, elle est, dans des conditions usuelles, négligeable bien que probablement observable (ce qui, il me semble, rejoint l’avis de l’académie des sciences).
J’ai l’impression que tu fais beaucoup de surinterprétation : tu juges la validité de certaines théories en dehors de leur cadre d’application, tu mélanges énormément de notions…
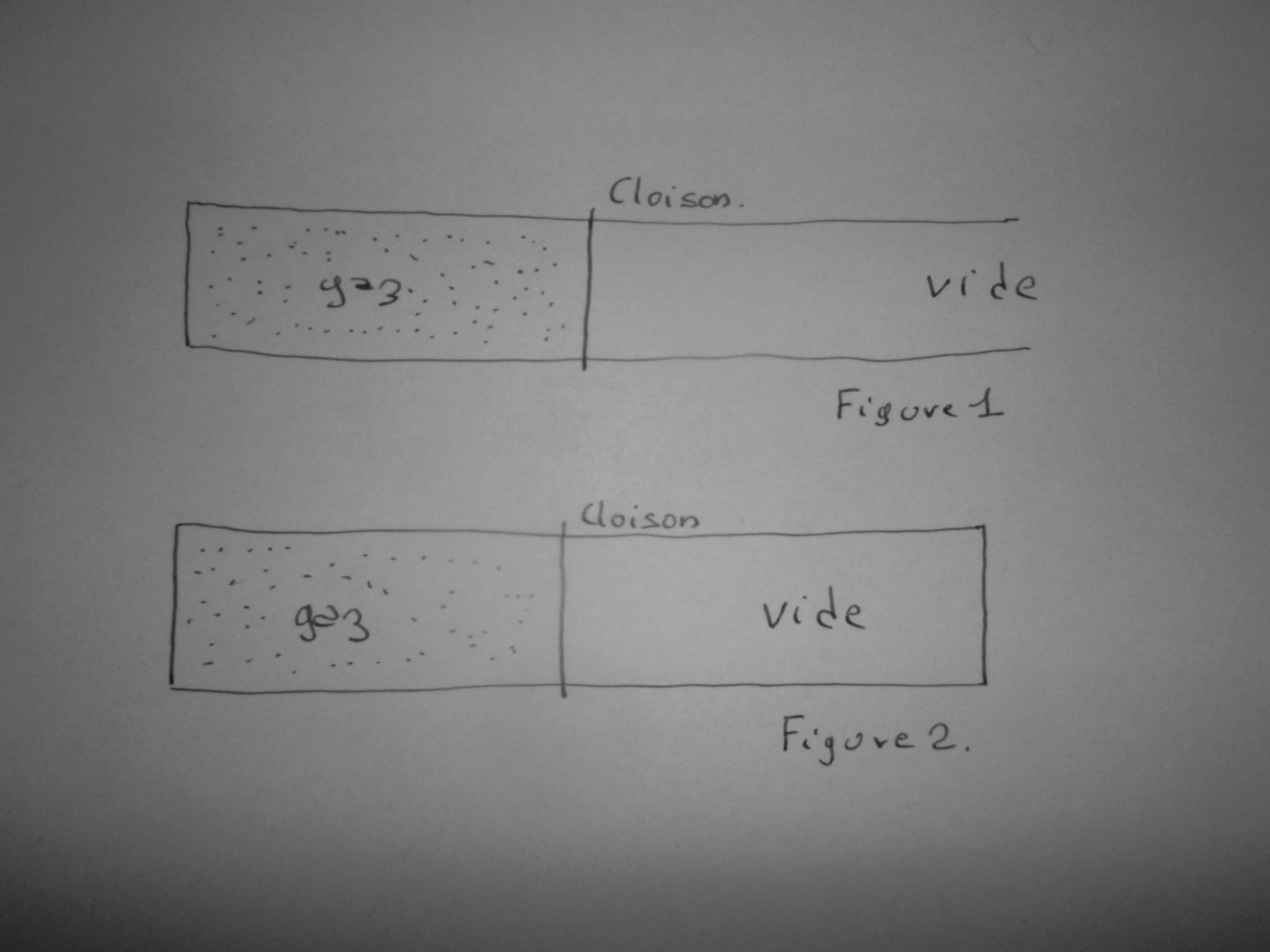
En plus, tu compliques les choses pour rien. Le cas de la détente d’un gaz dont la masse est de l’ordre de grandeur de celle du contenant est connu de tout le monde : c’est un ballon de baudruche qui se dégonfle brutalement ! Pas besoin de faire plein de calculs pour avoir une idée de son comportement.
 Dylan
Dylan