Le carbone 14 est une variété particulière de carbone utilisée pour dater des échantillons anciens, notamment pour l’archéologie. Le principe de la datation au carbone 14 est simple : on mesure la proportion de carbone 14 dans l’échantillon à dater, et on en déduit son âge. Pourtant, il y a de nombreuses étapes à franchir pour passer de la quantité de carbone 14 à l’âge de l’échantillon.
Cet article présente toutes ces étapes en commençant par présenter le cycle de vie du carbone 14, puis comment on peut mesurer le temps d’isolation d’un échantillon avec la décroissance radioactive, puis comment relier ce phénomène physique aux époques anciennes par calibration, avant d’expliquer comment on obtient en pratique une estimation d’âge avec cette technique de datation.
- Le carbone 14 et sa répartition sur Terre
- Mesure du temps par décroissance radioactive
- Le problème du rapport isotopique initial
- Aperçu de l'utilisation pratique de la courbe de calibration
Le carbone 14 et sa répartition sur Terre
Les isotopes du carbone
Comme tous les éléments chimiques, le carbone existe sous différentes variantes, qu’on appelle des isotopes. L’isotope le plus courant du carbone s’appelle le carbone 12, et c’est à lui qu’on pense quand on parle du carbone sans plus de précision. À l’état naturel, on ne rencontre sur Terre que trois isotopes du carbone : le carbone 12, qui en constitue 99%, suivi du carbone 13 pour 1%, le carbone 14 étant présent seulement à l’état de traces.
Ces quantités très différentes s’expliquent par la stabilité des différents isotopes. Le carbone 12 et le carbone 13 sont stables, ce qui signifie qu’ils resteront du carbone 12 et 13 aussi longtemps qu’on les observera. Le carbone 14, quant à lui, est instable : une fois produit, il se désintègre relativement vite et ne peut pas s’accumuler en grande quantité.
Cette désintégration est une réaction nucléaire au cours de laquelle le carbone 14 se transforme en azote et émet une radiation particulière : on dit que le carbone 14 est radioactif. Mesurer l’intensité de cette radiation est d’ailleurs un des moyens de connaître la quantité de carbone 14 dans un échantillon.
Production, répartition et disparition du carbone 14
Le carbone 14 présent sur Terre suit un cycle de vie de sa production à sa désintégration, qui permet de le répartir de manière inégale partout sur Terre.
Le commencement de ce cycle est la production de carbone 14 dans la haute atmosphère par l’action du rayonnement cosmique en provenance du Soleil sur l’azote. Cette réaction nucléaire est l’inverse de celle de la désintégration. L’activité du Soleil, et la production de carbone 14 associée, est variable.
Ensuite, le carbone 14 ainsi produit se répartit sur Terre, en se mêlant au cycle du carbone, dont la description serait bien trop vaste pour cet article. Ce cycle inclut par exemple l’intégration du carbone dans les plantes via le dioxyde de carbone, puis l’ingestion de plantes par des animaux, la vie de ces animaux, puis leur mort et l’intégration de leur carbone au sol ou retour de celui-ci dans l’atmosphère. Dans les océans, on a notamment la dissolution du dioxyde de carbone dans l’eau et son intégration dans le cycle de vie de l’océan, pour par exemple se retrouver dans la coquille de certains animaux marins.
Enfin, au fur et à mesure, le carbone 14 disparaît par désintégration radioactive. Cette désintégration, associée à des mécanismes de répartition complexes, aboutit à des quantités de carbone 14 différentes selon les milieux.
Une fois désintégré, le carbone 14 est devenu de l’azote. Ceci referme le cycle, puisque cet azote peut se retrouver dans la haute atmosphère où il pourra se transformer en carbone 14 sous l’effet du rayonnement cosmique !
Paramètres importants pour la datation
Les trois grandes étapes du cycle du carbone 14 sont sa production, sa répartition et sa désintégration, qu’il faut donc connaître pour être capable d’utiliser le carbone 14 comme moyen de datation précis. La désintégration est bien connue, c’est ce que nous présentons dans la section suivante. La production et la répartition sont plus difficiles à prendre en compte, on y parvient en réalisant une courbe de calibration, ce qui est présenté dans la section d’après.
Mesure du temps par décroissance radioactive
Échantillon isolé et décroissance radioactive
Puisqu’il se transforme spontanément en azote, le carbone 14 dans un échantillon a tendance à disparaître, lentement mais sûrement… sauf s’il est renouvelé au cours du cycle du carbone. Par contre, si on isole l’échantillon, c’est-à-dire si on le coupe du reste du monde, alors le carbone 14 ne sera pas renouvelé du tout, et sa quantité diminuera inexorablement en suivant des lois physiques bien déterminées ; c’est ce qu’on appelle la décroissance radioactive.
S’assurer que l’échantillon a été isolé pendant des centaines, voire des milliers d’années n’est pas évident du tout. Par exemple, un arbre mort échange très peu avec son environnement, mais sa décomposition peut tout de même aboutir à des échanges, à travers la vie des insectes xylophages, les colonies de bactéries, les précipitations, etc.
L’isolement de l’échantillon est une hypothèse très importante, puisque autrement il est impossible d’utiliser correctement les lois régissant la décroissance radioactive. Il n’est cependant pas forcément facile de l’établir.
Rapidité de la décroissance radioactive
La vitesse de la décroissance radioactive dépend de l’atome radioactif considéré. Comme pour tous les éléments radioactifs, la vitesse de décroissance du carbone 14 est mesurée à l’aide de la demie-vie. Pour le carbone 14, elle est de 5730 ans, ce qui signifie qu’au bout de ce temps, la moitié des atomes se sont désintégrés.
Pour bien comprendre ce que cela signifie, prenons un exemple. Si vous prenez une quantité initiale de carbone 14, vous n’aurez plus que :
- la moitié de la quantité initiale, soit 50%, après 5 730 ans (une demie-vie) ;
- la moitié de 50%, soit 25%, après 11 460 ans (deux demies-vies) ;
- la moitié de 25%, soit 12,5%, après 17 280 ans (trois demies-vies) ;
- et ainsi de suite jusqu’à la fin des temps.
On obtient ainsi une courbe de la forme suivante :
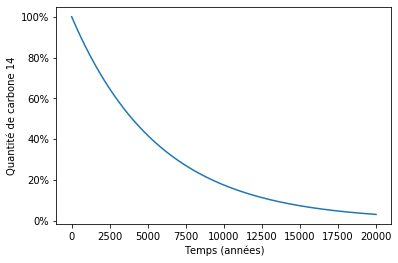
De la quantité au rapport isotopique de carbone 14
On s’intéresse en général plutôt à la quantité de carbone 14 relativement à tout le carbone présent dans un échantillon qu’à la quantité absolue de carbone 14. En effet, la quantité absolue de carbone 14 dépend de la taille de l’échantillon et de la quantité de carbone par rapport aux autres éléments. Exprimer les quantités en pourcentage permet de s’abstraire de toutes ces relations de proportionnalité. Par ailleurs, il existe des techniques de mesure très précises pour mesurer directement la proportion.
On peut même se contenter du rapport des quantités de carbone 14 par rapport au carbone 12, ce qu’on appelle le rapport isotopique C14/C12. Le ratio C14/C12 évolue de manière similaire à ce qu’on a vu précédemment, comme le montre la courbe ci-dessous.
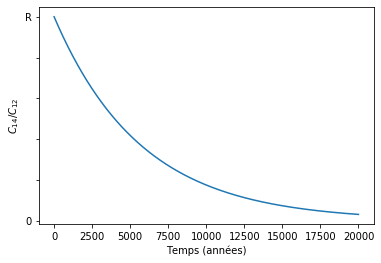
Cette courbe est l'esquisse d’une relation entre la quantité de carbone 14 dans un échantillon isolé et son âge ; elle ne suffit pas à elle toute seule à effectuer une datation.
En effet, si on connaît la concentration de carbone 14 initialement présente dans l’échantillon, on peut voir depuis quand cet échantillon a été isolé : il suffit de se placer à la quantité correspondante en ordonnée, puis de lire la date en abscisse. Il y a cependant un obstacle à franchir : il faut connaître la quantité de carbone 14 initialement présente dans l’échantillon…
Le problème du rapport isotopique initial
Variations du rapport isotopique
Le rapport isotopique initial est le résultat des mécanismes de production et de répartition du carbone 14 dans le passé, y compris à des époques très reculées.
Les valeurs du rapport isotopique C14/C12 des dernières décennies sont connues. En particulier, on a su estimer celui d’avant la seconde guerre mondiale, après quoi il a changé assez radicalement suite aux explosions nucléaires pratiquées par différents pays.
On pourrait penser que ce rapport était relativement constant avant d’être bouleversé par les humains, mais ce n’est pas le cas. En particulier, on a constaté des écarts assez importants entre la datation carbone 14 fondée sur un rapport isotopique supposé constant et celles issues de l’étude de la croissance des arbres, en particulier quand on remonte suffisamment dans le temps.
Il a donc fallu se rendre à l’évidence que la concentration entre carbone 14 de l’atmosphère varie sensiblement au cours du temps, et qu’il faut prendre cela en compte pour obtenir une datation précise. Même si j’insiste peu sur ce point dans l’article, il faut savoir que les concentrations en carbone 14 varient aussi en fonction du milieu (terrestre ou marin par exemple).
Réalisation de courbes de calibration
Il n’est malheureusement pas possible de déterminer précisément l’activité solaire et les flux de carbone dans le passé. On procède donc indirectement, en cherchant la correspondance entre des datations carbones « conventionnelles », établies par rapport à une concentration standard (celle de 1950) et des datations obtenues par d’autres moyens. Il est ainsi possible de se passer de la concentration isotopique pour corriger la datation obtenue.
Plusieurs études ont permis de collecter des données en différents endroits du globe. Les données de calibration de référence sont celles dites « IntCal » (la dernière version étant IntCal20) qui compilent différentes études, en particulier des arbres de l’hémisphère Nord. Ces études se basent sur la dendrochronologie, c’est-à-dire dire l’estimation de l’âge des arbres à partir de leurs cernes de croissance.
Le principe de calibration est le suivant :
- on prélève des échantillons dans des arbres variés ;
- on mesure l’âge de ces échantillons à l’aide des cernes (dendrochronologie) ;
- on effectue une datation au carbone 14 des cernes, en supposant le rapport isotopique égal à celui de 1950 ;
- on obtient alors une correspondance entre une datation au carbone 14 et une datation autre ;
- on procède ainsi sur quelques échantillons pour mitiger les variations statistiques.
À la fin, on obtient une courbe où, pour chaque datation au carbone 14, on peut déduire la vraie datation. La figure ci-dessous montre la courbe IntCal20 pour l’hémisphère Nord.
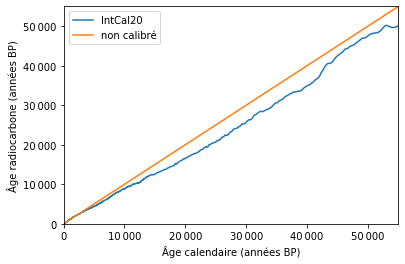
Comme la courbe de calibration (ligne bleue) est dessous la bissectrice (ligne orange), cela signifie que la datation au carbone non calibrée est systématiquement plus vieille que l’âge véritable obtenu par calibration. Par exemple, on voit qu’une datation carbone non calibrée qui donne environ 25 000 ans correspond en fait à 30 000 ans.
Aperçu de l'utilisation pratique de la courbe de calibration
Obtenir une datation non calibrée
Pour effectuer une datation au carbone 14, la première étape est de se doter d’un échantillon. Une fois cela fait, il s’agit de mesurer la proportion de carbone 14 dans cet échantillon et surtout la marge d’erreur associée.
Pour mesurer cette proportion, il existe deux techniques principales. La première consiste à mesurer la radioactivité de l’échantillon, mais c’est une technique longue, relativement imprécise et qui nécessite un échantillon assez gros. La deuxième consiste à utiliser un spectromètre de masse ; c’est une technique très précise et rapide, qui permet aussi d’utiliser de très petits échantillons. Cette mesure est associée à une incertitude notamment liée à la technique de mesure.
On peut ensuite déduire une datation non calibrée pour l’échantillon et la marge d’erreur associée, qu’il faudra calibrer.
Calibrer une datation
Pour obtenir l’âge calibré à partir de l’âge non calibré, il faut se servir de la courbe de calibration. C’est là que les choses se compliquent, à cause de la forme bosselée de la courbe de calibration et des marges d’erreurs.
Il existe différentes techniques d’estimation, mais je ne vais pas rentrer dans les détails, et utiliser celle proposée par un site à l’aspect désuet mais très pratique et sans inscription : http://calib.org/calib/calib.html.
Sur le site, j’ai saisi les données inventées suivantes (un seul échantillon donc) :
- âge radio carbone BP : 5300 ans (il s’agit donc d’une datation carbone non calibrée qui donne 5300 ans avant 1950) ;
- écart-type : 55 ans (valeur entièrement au hasard, ça dépend de plein de choses en pratique) ;
- courbe de calibration : IntCal20 (la dernière donc, même si pour cette date, la différence serait faible avec IntCal13).
En cliquant sur le gros bouton, le logiciel me donne un rapport avec l’image suivante :
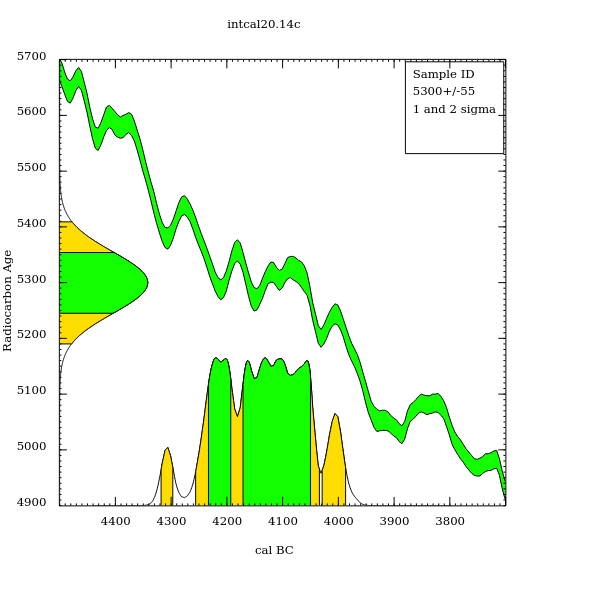
Le zigzag vert au milieu est la courbe de calibration avec les marges d’erreur. Par rapport à l’exemple donné précédemment, la courbe descend, car l’axe des abscisses est inversé.
Ensuite, on a une jolie gaussienne sur l’axe des ordonnées, qui correspond à la datation carbone non calibrée avec les marges d’erreurs. La couleur verte correspond à une plage à plus ou moins une fois l’écart-type ; le jaune marque la limite à plus ou moins deux fois l’écart type, puis blanc au-delà.
Enfin, on a une courbe toute cabossée sur l’axe des abscisses. C’est le résultat de la calibration ! On voit deux zones vertes (donc la zone qui correspond à une haute probabilité) : on a donc deux plages de dates distinctes probables pour une même mesure… Pas évident à interpréter sans données supplémentaires.
On voit que l’interprétation des datations peut être délicate, avec des traitements statistiques à effectuer et des plages d’incertitudes biscornues. Même si la datation au carbone 14 est presque routinière, elle n’est pas pour autant triviale !
Au-delà des considérations de cet article, de nombreux écueils existent en pratique. En effet, on ne date que le moment à partir duquel le carbone a cessé de se renouveler dans l’échantillon. Dans un contexte archéologique, par exemple, cela peut conduire à des interprétations fausses sans autres précautions. Par exemple, on peut vouloir dater une construction ancienne en bois, mais on date en fait la date à laquelle le bois a été coupé. Serait-il imaginable que le bois ait été recyclé d’une autre construction plus ancienne et donc ne corresponde pas à l’âge du bâtiment ?
Sources
- Carbon-14 sur Wikipedia.
- Radiocarbon dating sur Wikipedia.
- Radiocarbon calibration sur Wikipedia.
- Beta Analytic, un laboratoire de datation avec de nombreuses pages informatives.
- OxCal, un site web permettant des calibrations en ligne, gratuit, mais sur inscription.