Salut Blackline, voici comme promis quelques retours, sur la partie électron et intro générale. J’attends que la suite soit complétée pour la lire. Je confesse ne pas avoir lu tous les commentaires. Si je commente des points auxquels tu as déjà répondu, renvoies moi dessus. 
Intro générale
des liaisons
liaisons électroniques, je suppose (en plus, ça permet de parler d’électron dès le premier paragraphe)
Personnellement, Blackline, je vois la chimie quantique comme un outil intrinsèque pour comprendre les réactions de chimie organique.
Pourquoi « organique » en particulier ? Tu reviendras dessus par la suite ?
Pour la chimie quantique c’est un peu comme un zoom sur les électrons, ces électrons une fois en interaction au sein d’atome, ou au sein d’édifices plus grands comme les molécules, ils vont avoir un comportement très complexe et c’est au chimiste théoricien de s’y intéresser.
La phrase est tournée bizarrement. Je propose « La chimie quantique c’est un peu comme un zoom sur les électrons. Ces électrons, une fois en interaction au sein d’atome ou au sein d’édifices plus grands comme les molécules, vont avoir un comportement très complexe et c’est au chimiste théoricien de s’y intéresser. »
Mais les particules élémentaire ont un trait particulier qui les mettent hors de notre portée. C’est la dualité onde-corpuscule qui va nous empêcher de vraiment saisir la nature de ces particules.
Ma vision de la physique quantique me fait dire que la nature d’un électron est justement dual. Le problème, ce n’est pas que ce sont des objets hors de notre portée, c’est que ce ne sont pas des particules, justement.
L’idée dans ce tutoriel est de donné des pistes, voire des clés de compréhension pour observer comment, arrivons à travailler avec ces notions qui semblent souvent invraisemblables.
Je suppose que la bonne phrase est « L’idée dans ce tutoriel est de donner des pistes, voire des clés de compréhension, pour observer comment nous arrivons à travailler avec ces notions qui semblent souvent invraisemblables. » Même dans ce cas, observer comment on arrive à travailler, ça fait beaucoup de verbes à la suite.
Ortho :
vont-être -> vont être
esquive -> esquivent
au sein d’atome -> au sein d’atomes (édifices est au pluriel derrière)
leurs comportement -> leur comportement (ou leurs comportements)
les particules élémentaire -> les particules élémentaires
qui les mettent -> qui les met
est de donné -> est de donner
niveaux discret -> niveaux discrets
sont organiser -> sont organisés
Intro (L’électron)
C’est un peu le cœur de la physique quantique en fait : Que sont réellement les particules élémentaires et que savons-nous d’elles ? Dans les sphères d’études de la physique quantique on s’organise autour des particules élémentaire et de leurs comportements. L’idée est d’au moins pouvoir constater son comportement sans pouvoir voir ce que représente l’objet, .
Pas que « élémentaire ». On peut s’intéresser aux neutrons ou aux protons, par exemple. Sinon, dès qu’on fait de la physique quantique sur des objets un peu complexe, c’est la notion même d’objet composant qu’il faut oublier. Tu as un nuage d’électron ; c’est ÇA, ton objet, pas les électrons individuels eux-mêmes.
KLM…
Dans ce cas la lune sera accélérée autour de son orbite et commencerait à être attiré par la terre. Dans le modèle de Bohr, les orbites sont stationnaire et aucune énergie ne serait perdue en suivant cette trajectoire précise. Alors qu’en électromagnétisme classique un cas similaire obligerais l’électron à émettre de l’énergie. En fait l’électron ne peut pas être traité comme un objet classique "mais en plus petit".
Je sais parfaitement l’idée que tu veux faire passer, mais je trouve ce passage peu clair. Il faudrait que je retrouve comment on me l’avait présenté. Rien que l’idée que tout corps chargé en mouvement accéléré dans un référentiel galiléen émet de l’énergie n’est pas forcément intuitive (j’ai vu ça proprement… lorsqu’un prof nous a prouvé pourquoi le modèle de Bohr était insuffisant).
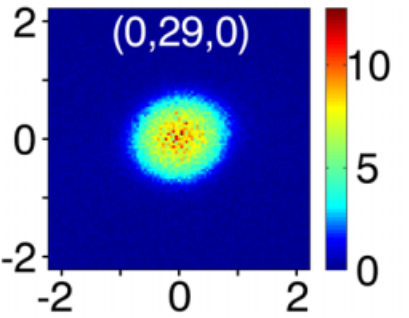
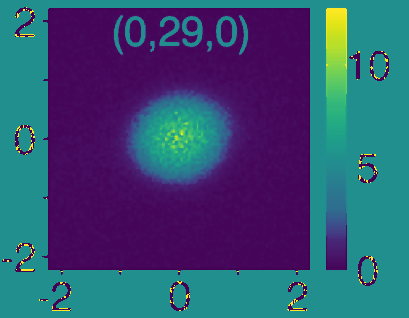
Densité de probabilité
Bien préciser dans la légende de la 1ère image à quoi correspond un « point ».
Forcément en recherchant dans tout l’espace connu et imaginable, on doit bien trouver au moins l’électron qu’on cherche. S’il était possible de minutieusement chercher à chaque portions de l’univers.
Pas « au moins ». Dans ce contexte, c’est un et un seul.
Pour ceux qui se demande pourquoi on se borne entre [0;+∞], c’est parce qu’une mesure de longueur négative n’a pas vraiment de sens en 3 dimensions.
C’est tout simplement qu’on intègre sur une sphère de centre le noyau et de rayon r. Le rayon ne peut pas être négatif. Si on avait intégré sur un cube dx dy dz, on intégrerait sur [-∞;+∞]3.
C’est en imaginant le rayon maximum tendant vers +∞ que l’on peut comprendre que l’on va prendre un volume supérieur à celui de la terre, du système solaire, plus grand que tout… Connaissant la taille d’un atome, effectivement si on achète l’univers entier, on y trouvera au moins 1 électron. Mais c’est une méthode démesurée  …
…
J’aime pas trop la formulation. On ne cherche pas un électron, mais l'électron, en considérant le système parfaitement seul dans l’univers. Et la probabilité que notre électron soit loin du noyau est faible. Et au-delà, il n’y a rien. Si on considère d’autres électrons, ton intégrale ne fera pas 1 (elle compte le nombre d’électron).
spdf
Les différentes Harmoniques Sphériques
Cette partie est mal organisée. On a la définition à la fin, les images au début. C’est peut-être parce que je ne suis pas chimiste, mais le tout est vraiment confus ici (mais je n’ai plus vu les spdf depuis le lycée), et j’ai bien du mal à suivre.
Règles de Klechkowsky
2 électrons maximum dans une orbitale
Ce n’était pas explicite avant.
Bon, j’ai raccroché avec les exemples dans la suite.
Spin
(Image) Vecteur borné sur un axe.
Je crains que ça ne laisse penser qu’un spin, selon comment il est projeté, puisse valoir moins qu’un demi (puisqu’on passe continument d’une borne à l’autre).
Zoom sur les nombres quantiques
Dans tes exemples, lorsqu’un seul spin est pris, ce peut être +1/2 ou -1/2. Comme tous tes exemples sont en +, ça laisse penser que ce n’est pas le cas.
Ortho : j’ai pas fait. 
Yop. J’attends que la suite soit écrite pour m’y atteler. À très vite. 
 Quand je ne met pas de source, les dessins sont de moi.
Quand je ne met pas de source, les dessins sont de moi. c’est corrigé
c’est corrigé




 ! Lors que l’héliporteur est attaqué par les contre-espions de Loki, une des hélices est endommagé et Iron + Captain america essaye de faire redémarrer cette hélice. Tony Stark donne demande à Steve Rogers de regarder les circuits ("Panneau contrôle moteur") pour lui dire quels relais sont en "position overload" et c’est ce qu’il dit :
! Lors que l’héliporteur est attaqué par les contre-espions de Loki, une des hélices est endommagé et Iron + Captain america essaye de faire redémarrer cette hélice. Tony Stark donne demande à Steve Rogers de regarder les circuits ("Panneau contrôle moteur") pour lui dire quels relais sont en "position overload" et c’est ce qu’il dit :
 (0%)
(0%)
