« Crise cardiaque » c’est une expression que nous n’aimons pas beaucoup utiliser en médecine : elle est trop vague. Même pour les patients, elle peut recouvrir plusieurs réalités différentes :
- certains auront en tête l’image du sportif qui s’écroule sans prévenir sur le terrain,
- pour d’autres c’est l’expression d’une douleur intense dans le thorax, au niveau du cœur,
- quelques patients enfin nous parlent de crise cardiaque en nous disant que « le cœur s’emballe ». C’est également assez imprécis mais ça désigne le plus souvent l’existence de palpitations (le fait de sentir son cœur battre, rapidement et de manière irrégulière).
Il existe d’autres exemples, mais rien que ces trois situations sont liées à trois pathologies très différentes.
Cet article vous propose de découvrir la prise en charge de l’une de ces détresses que l’on nomme couramment « crise cardiaque » mais dont le nom correct est Syndrome Coronarien Aigu (ou SCA). Pour ce faire, je vais m’appuyer sur le cas d’un vrai patient, anonymisé, vu lors d’une garde.
La nuit est tombée depuis quelques heures déjà au-dessus du bâtiment du SMUR1 dans lequel je prends mes gardes lorsque mon bip sonne, m’informant que mon équipage est sollicité pour partir en intervention. Dans cette joyeuse compagnie composée d’un médecin urgentiste, d’un infirmier et d’un ambulancier, je suis l’externe. Étudiant en médecine, pas vraiment nécessaire sur intervention, mais dont la présence est malgré tout appréciée, à la fois parce que les membres de l’équipe aiment enseigner mais également parce que je parviens à me rendre utile.
Pimpon. ♫
Et c’est reparti.
Vous l’aurez compris dès la lecture du titre, dans cet article nous allons parler du cœur ! Pour cela, je vous conseille la lecture du très bon Petit aperçu du fonctionnement cardiaque de @Goeland-croquant qui, s’il n’est pas nécessaire à la compréhension, sera malgré tout un complément précieux.
Vous vous demandez sans doute ce que représente le logo de l’article… Pas de panique, à la fin vous comprendrez.
- Dans un département il existe un SAMU (Service d’Aide Médicale d’Urgence) qui réceptionne les appels au 15. Si la détresse est grave et dépasse le niveau secouriste, le SAMU va solliciter un des SMUR (Structure Mobile d’Urgence et de Réanimation) du département pour envoyer un médecin sur place. Le SMUR est un service hospitalier dans lequel les équipages médicaux (ou paramédicaux) sont de garde et se déplacent sur consigne du SAMU, généralement dans des camions tout équipés que l’on appelle des UMH (Unité Mobile Hospitalière).↩
Une chance sur dix
L’intervention
Notre motif de départ : douleur thoracique chez un patient de 70 ans. Très classique en SMUR, puisque cela représente à peu près 30% de nos interventions. Dans la majorité des cas, les douleurs sont bénignes mais l’exclusion des diagnostics graves nécessite des examens complémentaires et une interprétation qui ne peuvent se faire sans un médecin.
Arrivée sur place. Les secouristes sont déjà présents et ont commencé leur bilan.
La coordination des services de secours n’est pas la même dans tous les départements. Dans le mien, les pompiers (ou secouristes) sont envoyés en première intention de manière quasi systématique. Si le cas est grave, un renfort SMUR part sur intervention, soit dès le départ (si le médecin régulateur identifie la gravité au téléphone) soit secondairement, demandé par les pompiers. Chacun des équipages dispose de la possibilité d’évacuer la victime : si le cas est grave, c’est le SMUR qui évacue (parce que surveillance médicale nécessaire). S’il ne l’est pas, les pompiers évacuent pour libérer l’équipage SMUR (parce qu’il y a beaucoup moins de SMUR disponibles que de pompiers).
Le bilan des secouristes leur permet déjà d’exclure un certain nombre de détresses graves : le patient est conscient, il ventile (terme médical pour dire qu’il respire) correctement et il est hémodynamiquement stable, c’est-à-dire que, quelle que soit sa pathologie, pour le moment elle n’a pas d’incidence sur la capacité de son cœur à vasculariser les autres organes. Il faut dire que le patient est au repos et que tout est fait pour lui éviter le moindre effort afin que le cœur ne se retrouve pas en difficulté s’il était atteint. Finalement, le seul élément sortant de la normale qu’ils retrouvent, c’est la douleur du patient : rétrosternale (en arrière du sternum, l’os au centre du thorax), compressive (comme un étau), intense et irradiant vers le bras gauche.
Pour le moment le patient est sur le palier (très étroit) du 3e étage, là où il a été retrouvé. Son appartement étant inaccessible et devant l’absence manifeste de signes de gravité, le médecin décide qu’il soit brancardé jusque dans un véhicule pour continuer l’examen dans de meilleures conditions. C’est le camion des secouristes qui sera choisi puisque, comme me l’explique le médecin, même si la douleur décrite est assez typique d’une origine cardiaque, le reste de l’examen est très rassurant et le patient ne déclare aucun facteur de risque cardiovasculaire. Il estime ainsi la probabilité que ce soit bénin à 9 chances sur 10.
Une fois la victime confortablement installée dans le camion des secouristes, ces derniers nous laissent la place pour que nous commencions l’examen médical. Le temps fort de cet examen, c’est la réalisation d’un ECG qui nous permet de détecter certaines anomalies cardiaques.
L’électricité du cœur
Un peu de physiologie
La contraction cardiaque est le fruit d’une succession de trois événements :
- Un premier événement électrique. Il existe au sein du cœur une région particulière appelée le nœud sinusal et dont le rôle est de délivrer un signal électrique à une fréquence régulière. À l’état basal, les cellules cardiaques sont dites polarisées, c’est-à-dire qu’elles ont un certain potentiel électrique. Le signal émis par le nœud sinusal provoque une dépolarisation des cellules, c’est-à-dire une modification de leur potentiel. Cette onde de dépolarisation est transmise par le biais de faisceaux spécialisés mais également de proche en proche : d’une cellule à sa voisine.
- Un deuxième événement chimique. La dépolarisation de la cellule va entraîner la libération de calcium contenu dans une zone particulière de la cellule qui s’appelle le réticulum sarcoplasmique. Le calcium va venir se lier à la troponine, une protéine dont la liaison avec le calcium entraîne un changement de conformation (autrement dit, elle change de forme).
- Un troisième événement mécanique. En changeant de conformation, la troponine cardiaque permet à deux autres protéines de se lier : l'actine et la myosine. Ces deux protéines forment des structures semblables à des ponts qui vont d’une extrémité à l’autre de la cellule. En se liant à l’actine, la myosine va « tirer dessus » et entraîner un raccourcissement de celle-ci. Le raccourcissement simultané de tous les ponts actine-myosine de la cellule entraîne un raccourcissement de la cellule elle-même (de quelques micromètres). Synchronisées par le signal électrique, toutes les cellules contractiles du myocarde (le muscle cardiaque) se raccourcissent en même temps, aboutissant à la contraction du cœur.
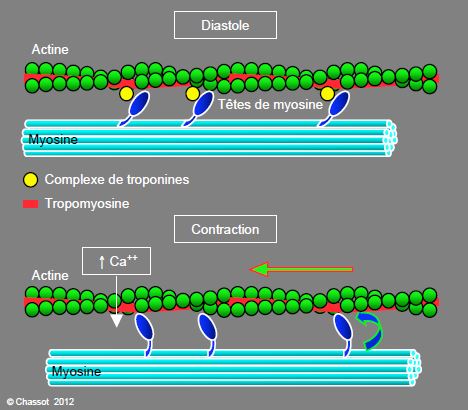
Ces trois événements sont liés entre eux : tout trouble du fonctionnement électrique va entraîner un trouble du fonctionnement mécanique et inversement (sauf dans le cadre d’une pathologie rare qui s’appelle la Dissociation Électro-Mécanique). L'ECG qui est un enregistrement électrique du cœur est donc un excellent examen pour voir comment celui-ci fonctionne.
Faire un bel ECG
L'ECG classique présente 12 dérivations. Autrement dit, on observe l’activité électrique du cœur depuis 12 points de vue différents qui permettent chacun de détecter des anomalies que ne voient pas les autres. Ces 12 dérivations sont obtenues grâce à 10 électrodes collées sur la peau du patient :
- 4 électrodes frontales ou périphériques placées chacune sur un membre. Ces électrodes permettent d’observer l’activité électrique sur un plan frontal, c’est-à-dire parallèle au front et coupant le corps en deux parties, une partie antérieure et une partie postérieure. De ces 4 électrodes naissent 6 dérivations, 3 dérivations bipolaires (différence de potentiel entre deux électrodes) et 3 dérivations unipolaires (différence de potentiel entre une électrode et le centre électrique du cœur). La quatrième électrode (celle du membre inférieur droit) n’a qu’une utilité technique.
- 6 électrodes précordiales, placées sur le thorax à des endroits précis. Ces électrodes permettent d’observer le cœur dans un plan transversal, c’est-à-dire traversant le corps d’avant en arrière, le séparant ainsi en une partie supérieure et une partie inférieure. Ces 6 électrodes donnent 6 dérivations unipolaires.
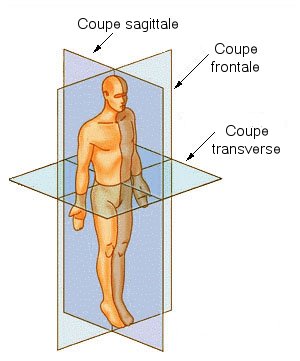
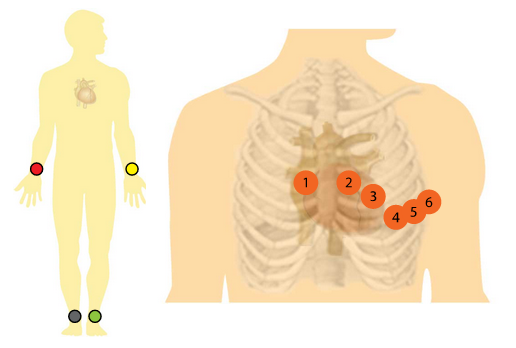
Comme vous pouvez le constater, sur le plan transversal, les électrodes sont majoritairement localisées à gauche du patient. En effet, anatomiquement, le cœur est au centre du thorax et dépasse des deux côtés du sternum, mais il dépasse de manière plus importante sur la gauche que sur la droite. De plus, la zone la plus importante pour son fonctionnement est le ventricule gauche, logiquement situé à gauche.
Toutefois, pour la douleur thoracique, on a besoin de voir l’intégralité du cœur. On va donc recourir à un ECG 18 dérivations qui rajoute par rapport à l'ECG 12 dérivations classiques :
- 2 dérivations pour observer le cœur droit,
- 3 dérivations pour observer le cœur postérieur.
Mais 12 + 2 + 3, ça fait 17, non ?
En effet, jeune padawan cardiologue. La 18e dérivation n’est jamais utilisée en pratique clinique, mais on persiste malgré tout à appeler cet examen un ECG 18 dérivations pour des raisons historiques.
Lire l'ECG
Lire correctement un ECG ça demande plusieurs heures de cours et des centaines d’heures de pratique (et on ne parle là que d’une lecture basique), il n’en est pas question ici. Toutefois, je vous propose malgré tout que l’on voie ensemble à quoi ça ressemble et quelles sont les conséquences sur son tracé de la pathologie que nous cherchons.
Où va le courant ?
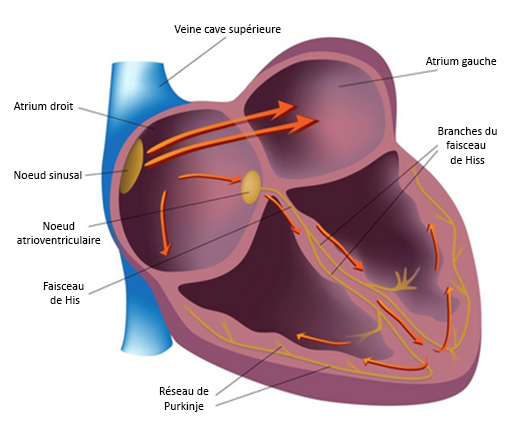
Le cœur est constitué de deux parties :
- Le cœur gauche (situé à droite sur le schéma), la partie la plus volumineuse et la plus importante. Il est chargé de récupérer le sang oxygéné en provenance des poumons pour l’envoyer vers le reste de l’organisme.
- Le cœur droit (situé à gauche sur le schéma). Il récupère le sang désoxygéné revenant des organes et le renvoie vers les poumons pour le réoxygéner.
Chaque moitié du cœur est elle-même constituée de deux cavités :
- une chambre d’admission appelée atrium (ou oreillette),
- une chambre d’expulsion appelée ventricule.
Le signal électrique naît au niveau du nœud sinusal qui est situé proche de l’arrivée de la veine cave supérieure (l’une des deux veines qui amènent le sang dans l’atrium droit). Ce signal électrique va d’abord parcourir les deux atriums et y provoquer une dépolarisation, donc une contraction bi-atriale simultanée.
Dans le même temps, l’impulsion va rejoindre un second nœud : le nœud atrio-ventriculaire par lequel va passer le signal pour pouvoir aller des atriums aux ventricules. En effet, chaque atrium est isolé électriquement de son ventricule afin d’obliger le signal à passer par le nœud atrio-ventriculaire (et quand l’isolation n’est pas parfaite, cela donne des pathologies). Ce passage obligé permet au cœur de retarder de quelques millisecondes la transmission du signal aux ventricules pour permettre à la contraction atriale de se terminer avant que ne commence la contraction ventriculaire.
Après cette période de pause, le signal emprunte le faisceau de His qui se divise en plusieurs branches, chaque branche donnant naissance à de petites terminaisons nerveuses éparpillées dans le myocarde qui forment le réseau de Purkinje (se lit « purkineyé »). Cette organisation en réseau permet à la dépolarisation de parcourir l’intégralité des ventricules à très grande vitesse et donne ainsi une dépolarisation simultanée des deux ventricules.
Et sur le papier, ça donne quoi ?
Si on isole un cycle cardiaque sur une dérivation (en l’occurrence, V6), on obtient ce genre de tracé.
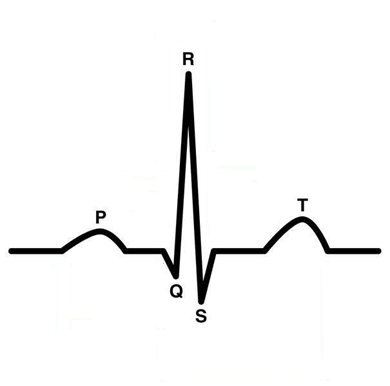
La ligne de base est appelée ligne isoélectrique. Chaque déflexion positive ou négative est appelée une onde.
Toutes les ondes ont été baptisées d’un petit nom. La première onde est de faible intensité et d’apparence arrondie. C’est l’onde P et elle correspond à la dépolarisation bi-atriale.
Ensuite, il y a un ensemble de trois ondes de morphologie plutôt triangulaire, Q, R et S, baptisé le complexe QRS. Le complexe QRS représente la dépolarisation bi-ventriculaire.
Afficher/Masquer le contenu masqué
On peut se demander pourquoi le QRS a une forme aussi complexe alors que l’onde P est plutôt simple. La réponse nécessite de comprendre un peu mieux comment l’électrocardiographe (la machine qui réalise les électrocardiogrammes) réalise ses mesures. Notez que cette explication n’est pas nécessaire pour comprendre la suite de l’article, considérez-la comme du bonus.
La dérivation que je vous ai présentée correspond à V6, c’est-à-dire la 6e électrode précordiale. Si vous remontez jusqu’au schéma de positionnement des électrodes, vous constaterez que de toutes les électrodes précordiales, V6 est la plus à gauche et la plus en bas.
L’état basal (cellule polarisée) est représenté par la ligne isoélectrique. Chaque déflexion positive représente une onde qui se rapproche de l’électrode et chaque déflexion négative représente une onde qui s’éloigne de l’électrode.
La conduction atriale peut être résumée en un seul vecteur qui part du nœud sinusal pour aller vers le nœud atrio-ventriculaire. Or, si vous regardez le schéma anatomique du cœur que je vous ai mis un peu plus haut, vous verrez que ce trajet est vers la gauche et vers le bas… donc vers V6 ! La dépolarisation atriale se dirige vers V6 et donc l’onde P est une déflexion positive. La contraction atriale n’est pas très puissante, l’intensité de l’onde (sa hauteur) est donc plutôt faible.
Au contraire, la conduction intra-ventriculaire ne peut pas être résumée à un seul vecteur mais en nécessite trois (d’où trois ondes !) :
- Un premier vecteur septal qui va dépolariser le septum inter-ventriculaire, c’est-à-dire la paroi entre les deux ventricules. Cette dépolarisation est dirigée vers le bas et vers la droite et elle est de faible intensité d’où une petite onde q négative en V6.
- Un second vecteur gauche qui va dépolariser la pointe du cœur (apex) et le ventricule gauche. Cette dépolarisation est la plus importante (car le ventricule gauche est le plus puissant) et se dirige vers le bas et vers la gauche. Elle donne donc une onde R positive et très haute en V6. (En réalité, le vecteur gauche est lui-même composé de deux vecteurs, un vecteur apical et un vecteur pariétal, mais ça complexifie un peu trop l’explication…)
- Un troisième vecteur droit qui dépolarise le ventricule droit. La dépolarisation est plus faible que celle du ventricule gauche (car le ventricule droit se contracte moins : il y a besoin de moins de puissance pour envoyer le sang dans les poumons qui sont à côté que pour l’envoyer dans tout l’organisme et notamment au cerveau qui nécessite de vaincre la gravité). Elle est dirigée vers la droite et vers le haut (vers le haut, car elle part de l’apex pour remonter sur le ventricule droit). Tout cela donne donc une onde négative et de moyenne intensité en V6.
L’association de ces trois vecteurs donne ainsi le complexe QRS.
La dénomination des ondes du complexe QRS est fixe : l’onde Q est toujours la première déflexion négative, l’onde R toujours l'unique déflexion positive et l’onde S toujours la dernière déflexion négative. La morphologie des QRS varie d’une dérivation à une autre : en V1 par exemple, il est fréquent de ne pas voir la première déflexion négative (l’onde Q). Dans ce cas, on dit qu’on ne voit pas d’onde Q et que la première onde (positive donc) est une onde R.
Il peut exister des variations dans lesquelles il y a par exemple plusieurs déflexions positives dans un QRS, mais elles sont pathologiques.
Entre l’onde P et le complexe QRS, il existe une zone où le potentiel revient à la ligne isoélectrique. Cette zone est baptisée le segment PR (PR plutôt que PQ car, comme on l’a vu juste avant, l’onde Q n’est pas systématiquement vue). Le segment PR représente le retard introduit par le nœud atrio-ventriculaire entre la dépolarisation atriale et la dépolarisation ventriculaire dont je vous ai parlé précédemment.
La dernière onde est l'onde T, d’une morphologie un peu similaire à l’onde P mais de plus grande intensité en règle générale. Entre le complexe QRS et l’onde T se situe le segment ST. L’ensemble segment ST + onde T représente la repolarisation ventriculaire (le segment ST c’est la repolarisation ventriculaire lente et l’onde T c’est la repolarisation ventriculaire rapide).
Il existe aussi une repolarisation atriale, mais c’est un tout petit événement électrique qui prend place pendant la dépolarisation ventriculaire. L’onde correspondante est invisible, noyée dans le complexe QRS.
L'ECG 12 dérivations
Voilà à quoi ressemble un ECG complet :
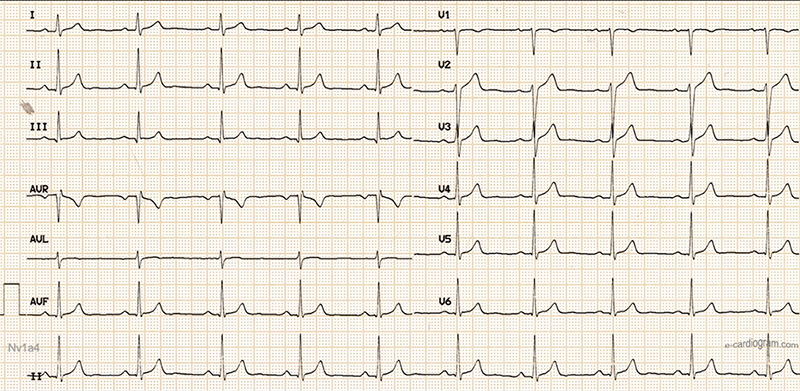
L’enregistrement dure 10 secondes et tous les événements situés au même niveau sur l’axe des abscisses ont lieu en même temps, quelle que soit leur dérivation.
Et notre patient alors ?
Après cette petite digression, vous savez à peu près à quoi ressemble un ECG normal. Notre patient lui présente une anomalie que l’on appelle un sus-décalage du segment ST. C’est une anomalie très grave dont nous allons discuter dans la suite. Le patient est donc transféré dans notre véhicule afin d’être médicalisé.
C’était la mauvaise chance sur dix.
C'est quoi SCA ?
Et ça décale
Sachez qu’il existe des dizaines et des dizaines d’anomalies possibles. Chaque onde, chaque segment, chaque intervalle (une entité dont je ne vous ai pas parlé), peut être trop long, trop court, trop intense, trop faible, avoir un aspect inhabituel… Et certaines de ces anomalies peuvent se combiner entre elles pour former des anomalies plus complexes.
Bref, tout ça pour vous dire qu’on va se focaliser sur une de ces anomalies et ce sera déjà pas mal ! L’anomalie en question, c’est le sus-décalage du segment ST dont j’ai commencé à vous parler dans la fin de la partie précédente.
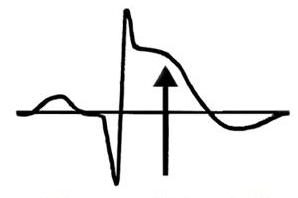
En temps normal, le segment ST (situé entre l’onde S - dernière onde du complexe QRS - et l’onde T) est au niveau de la ligne isoélectrique. Comme vous pouvez le constater sur l’image plus haut, il est ici sus-décalé. Ainsi que nous l’avons vu il y a quelques paragraphes, le segment ST représente la repolarisation lente. Le sus-décalage du segment ST appartient donc à la famille des troubles de la repolarisation.
Le sus-décalage du segment ST est un signe ECG très important qui signale une pathologie que l’on appelle le Syndrome Coronarien Aigu (ou SCA).
Il existe plusieurs morphologies de sus-décalages, toutes n’indiquant pas un SCA. Toutefois, dans le cadre de cet article, nous allons en rester à sus-décalage de ST = SCA.
De la même manière, il existe deux types de SCA :
- le SCA avec sus-décalage du segment ST, appelé SCA ST+ (ou STEMI en anglais pour ST Elevation Myocardial Infarction),
- le SCA sans sus-décalage du segment ST, appelée SCA ST- (ou NSTEMI en anglais, Non ST Elevation Myocardial Infarction).
Le SCA ST+ est le plus grave !
Coronarien ?
Comme tous les organes, le cœur a besoin d’oxygène pour fonctionner correctement. Cet oxygène lui est apporté par le biais de deux artères que l’on appelle les artères coronaires.
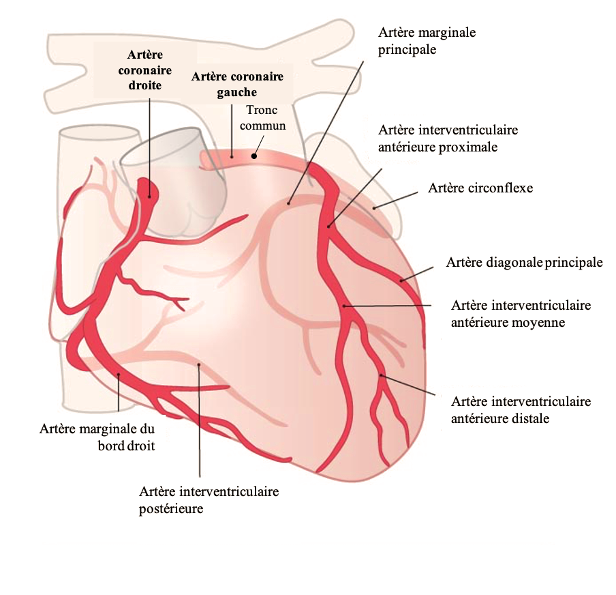
Il existe donc une artère coronaire gauche et une artère coronaire droite qui se divisent toutes les deux en une multitude de branches. Ces artères naissent de l’aorte, directement à la sortie du ventricule gauche.
Quand un caillot se forme et vient boucher l’une de ces artères (ou l’une des branches de l’artère), une partie du cœur n’est plus correctement vascularisée et va très rapidement commencer à souffrir. C’est un Syndrome Coronarien Aigu.
L’artère du cœur qui se bouche, ce n’est pas ça qu’on appelle un infarctus du myocarde ?
Pas tout à fait, mais il faut dire que la nuance entre le SCA et l'IdM est assez subtile, à tel point qu’on a tendance à les utiliser facilement l’un à la place de l’autre.
Mais si on veut être très précis, un infarctus du myocarde est une nécrose du tissu musculaire cardiaque, c’est-à-dire une mort des cellules qui le composent créant ainsi dans le cœur une zone qui ne fonctionnera plus jamais et que l’on appelle la zone infarcie.
Par conséquent, l’insuffisance brutale d’apport d’oxygène au myocarde causée par un caillot est un SCA. Dans un second temps, si l’insuffisance persiste, les cellules vont commencer à nécroser, donnant ainsi un IdM. En toute rigueur, l'IdM est une conséquence du SCA, toutefois, le myocarde est tellement sensible au manque d’oxygène que la nécrose peut apparaître en quelques minutes seulement (15 à 30 en général) ! En raison de cette rapidité, on confond usuellement SCA et IdM.
Comment se forme un caillot ?
La réponse tient en un mot : athérosclérose. Connue du grand public sous le nom un peu réducteur de cholestérol, l’athérosclérose désigne la formation progressive (sur plusieurs dizaines d’années) de plaques d’athérome au sein de la paroi des grosses et moyennes artères. Ces plaques vont amener petit à petit à la réduction du calibre des artères où elles prennent place et donc à un passage de plus en plus difficile du sang. Elles sont principalement composées de cholestérol (un lipide), d’où la confusion de nommage.
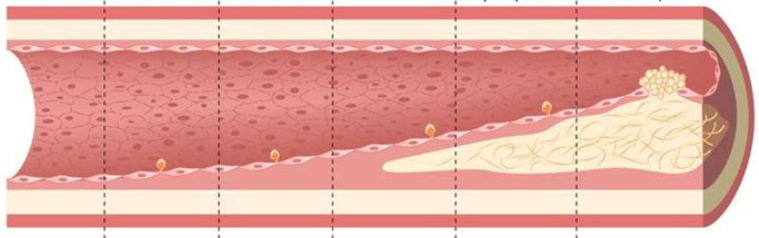
On entend souvent parler de bon cholestérol et de mauvais cholestérol. Ce n’est pas tout à fait vrai : le cholestérol est un lipide dont il n’existe qu’une seule version. En revanche, ce qui change ce sont les transporteurs sanguins du cholestérol (de la famille des lipoprotéines). Il en existe deux :
- LDL (Low Density Lipoprotein) ou « mauvais cholestérol » qui favorise l’accumulation du cholestérol dans la paroi artérielle,
- HDL (High Density Lipoprotein) ou « bon cholestérol » qui, au contraire, permet d’éviter cette accumulation.
Quoi qu’il en soit, l’évolution que nous venons de décrire est chronique avec l’apparition très progressive de symptômes, au début peu handicapants, mais qui progressent doucement, laissant le temps au patient de consulter son médecin traitant qui le renverra vers un cardiologue pour le mettre sous traitement.
Ça ne correspond pas vraiment à la situation de notre patient et c’est normal. Le SCA ST+ est une complication d’une autre nature de l’athérosclérose, beaucoup plus urgente. En grossissant, une plaque d’athérome peut devenir instable à force d’être confrontée au flux sanguin artériel. En effet, la circulation artérielle est pulsatile (rythmée par les contractions cardiaques) et cette pulsatilité « tape » sur les plaques d’athéromes, entraînant des lésions et des ruptures.
La plaque étant logée dans la paroi artérielle, quand elle se rompt le corps humain va réagir de la même façon que pour une rupture de paroi : il va tenter de combler le trou. Un bouchon (appelé caillot ou thrombus) se forme, composé de plaquettes et de fibrine. Ce thrombus grossit et bloque la circulation sanguine sur place, c’est la thrombose. Contrairement à la constitution de la plaque qui prend plusieurs dizaines d’années, la formation du thrombus se fait sur quelques dizaines de minutes à quelques heures, d’où l’apparition brutale des symptômes. Quand cette thrombose se produit dans une artère coronaire, on appelle cela un SCA.
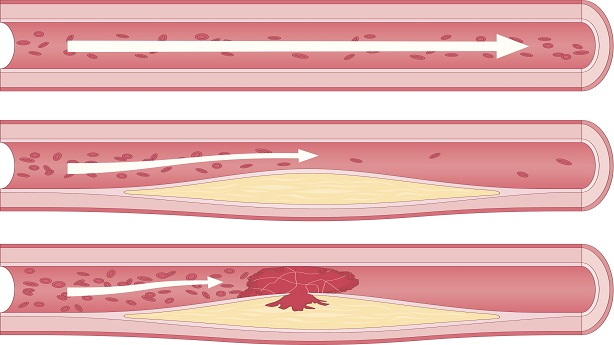
L’athérosclérose est donc à la base de la physiopathologie du SCA et nous ne sommes pas tous égaux face à son développement. En effet, elle est favorisée par un certain nombre de facteurs de risques. Il existe tout d’abord des facteurs de risque non modifiables :
- l'âge, plus on est âgé et plus on est à risque,
- le sexe, les hommes sont plus à risque que les femmes,
- l'hérédité, vous êtes plus à risque s’il y a déjà eu thromboses artérielles dans votre famille. Notez que ces thromboses peuvent être cardiaques (SCA), cérébrales (AVC), ou autres.
Comme leur nom l’indique, ces facteurs de risque ne peuvent être modifiés, il est donc impossible d’agir dessus. Il existe cependant des facteurs de risques modifiables auxquels on peut faire attention pour minimiser son risque vasculaire :
- Le tabagisme, qui diminue le taux d’HDL-cholestérol (le « bon cholestérol »).
- l'hypercholestérolémie, une maladie qui favorise elle aussi le LDL-cholestérol au détriment du HDL-cholestérol. Le plus souvent liée à une prédisposition génétique et à l’alimentation (surtout riche en acides gras saturés).
- l'hypertension artérielle. Quand la pression artérielle d’un patient augmente, son risque cardiovasculaire augmente avec.
- le diabète, en particulier le diabète de type 2.
Le diabète sucré (le plus souvent appelé simplement diabète) est une pathologie dans laquelle les patients ne sont plus capables d’absorber les sucres présents dans le sang, ce qui mène à une hyperglycémie. Il en existe deux types principaux :
- Le diabète de type 1, lié à une destruction des cellules pancréatiques (les cellules β) qui synthétisent l’insuline, l’hormone qui permet aux cellules d’absorber le sucre. C’est un diabète qui se déclare généralement chez l’enfant.
- Le diabète de type 2, lié à une résistance acquise à l’action de l’insuline par saturation du sang en sucres. Se développe le plus souvent chez l’adulte, en particulier l’adulte en surpoids, sédentaire avec un régime alimentaire gras et sucré.
Il en existe d’autres types, plus rares.
- l'obésité abdominale dite androïde car elle se développe plus fréquemment chez l’homme que chez la femme qui est plutôt sujette à l’obésité gynoïde (cuisses et fesses),
- certains facteurs psychosociaux, notamment le stress.
À l’inverse, il existe des facteurs protecteurs :
- la consommation de fruits et légumes,
- l'activité physique,
- la consommation modérée d’alcool (voire l’absence de consommation).
Comment est-il possible que notre patient ait développé un SCA alors qu’il ne nous a déclaré aucun facteur de risque ? Eh bien rien n’est impossible dans l’absolu, c’est juste extrêmement rare. Le plus probable, toutefois, c’est que le patient n’ait pas connaissance de ses facteurs de risque. Manifestement en rupture de suivi médical1, il est fort possible qu’il soit hypertendu, diabétique ou dyslipidémique (une autre façon de dire qu’il souffre d’hypercholestérolémie) et qu’il l’ignore. Voire une combinaison de plusieurs de ces facteurs.
- Je ne l’ai pas précisé avant parce que ça n’a pas forcément de plus-value dans la prise en charge aiguë, mais outre son problème cardiaque, le patient présentait une incurie (le fait de ne pas prendre soin de soi), une syllogomanie (syndrome d’accumulation compulsive) qui expliquait l’impossibilité d’accéder à son appartement ainsi que d’autres symptômes. Le tout formait un contexte psychiatrique qui est souvent compatible avec l’apparition de facteurs de risque cardiovasculaires et l’absence de consultation chez un médecin.↩
Traitons !
Rappel des faits : notre patient est dans le camion du SAMU et nous lui avons diagnostiqué un SCA à l'ECG. Il n’y a pas besoin d’examen diagnostique supplémentaire : le sus-décalage du segment ST nous permet d’affirmer le SCA ST+ et à partir de là, la prise en charge en secteur hospitalier devient une urgence absolue.
Transport
Le but du SMUR, au-delà de poser le diagnostic, c’est aussi de transporter le patient en vie jusqu’à l’hôpital. La première chose, c’est qu’il est absolument indispensable que le patient ne bouge pas et ne fasse aucun effort. Pourquoi ? Faire un effort reviendrait à augmenter la consommation en oxygène du cœur alors que celle-ci n’est déjà pas suffisante au repos. La dégradation serait encore plus rapide.
En urgence et avant même l’arrivée à l’hôpital, on va administrer au patient une trithérapie antithrombotique (anti formation de thrombus si vous préférez). Ça ne va pas dissoudre le caillot, mais ça va permettre d’éviter qu’il ne grossisse encore. Cette trithérapie est constituée de deux antiagrégants plaquettaires et d’un anticoagulant, permettant ainsi de contrer toutes les étapes de l’hémostase.
L'hémostase c’est le processus qui permet la réparation des vaisseaux sanguins (et c’est également celui qui est à l’œuvre dans la formation du thrombus qui obstrue notre artère). Il est composé de trois étapes :
- L'hémostase primaire qui consiste en une agrégation des plaquettes pour former ce qu’on appelle un clou plaquettaire. Les antiagrégants viennent s’y opposer.
- La coagulation est une cascade biochimique complexe qui aboutit à la formation de fibrine. La fibrine complète le clou plaquettaire pour former un thrombus. Les anticoagulants sont efficaces ici.
- La fibrinolyse, c’est la dissolution du caillot une fois que la réparation vasculaire est définitive. Nul besoin de la contrer ici, bien au contraire.
Le patient est scopé, c’est-à-dire relié à un appareil qui permet de surveiller en direct ses paramètres vitaux (saturation du sang en oxygène, tension artérielle, rythme cardiaque, etc.) et on lui pose même les électrodes du défibrillateur en préventif. En effet, la probabilité d’arrêt cardiaque est loin d’être négligeable.
Il n’y a qu’une seule destination possible pour ce type de pathologie : l'Unité de Soins Intensifs de Cardiologie ou USIC afin de rétablir la circulation au sein de l’artère, c’est ce que l’on appelle une reperfusion.
Localiser le caillot
C’est bien de beau de vouloir reperfuser l’artère, mais laquelle (il y en a deux !) ? Et à quel niveau ? Il va donc falloir localiser précisément la lésion.
Dans un but de débrouillage, l'ECG peut nous aider. En effet, souvenez-vous que chaque électrode permet d’observer le cœur sous un angle différent. Or, le sus-décalage du segment ST n’est pas présent sur toutes les dérivations : il n’est présent qu’en regard des dérivations qui pointent vers une portion du cœur qui souffre !
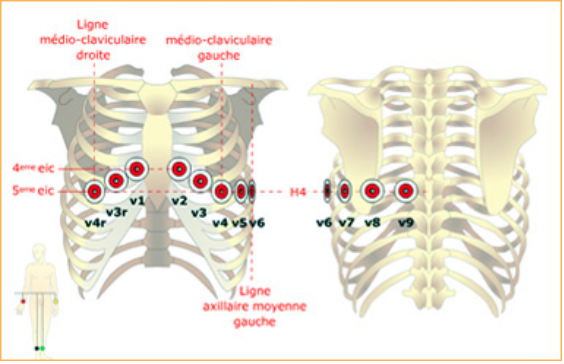
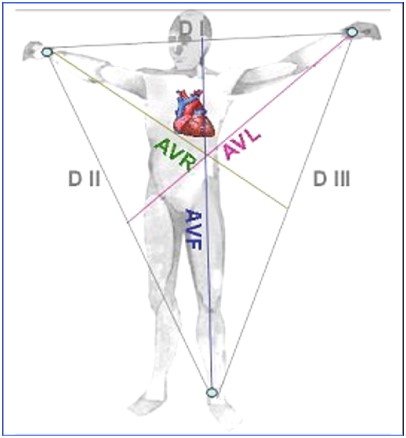
En plus de voir où sont situées les dérivations supplémentaires de l'ECG 18 dérivations, je vous montre aussi exactement comment sont définies les dérivations du plan frontal. Comme je vous l’avais expliqué, il existe 3 dérivations bipolaires (différence de potentiel entre deux électrodes) :
- DI, entre les deux électrodes des membres supérieurs ;
- DII, entre le membre supérieur droit et le membre inférieur gauche ;
- DIII, entre le membre supérieur gauche et le membre inférieur gauche.
Il existe également 3 dérivations unipolaires (différence de potentiel entre une électrode et le centre du cœur qui est un point théorique) :
- aVR, avec l’électrode du membre supérieur droit ;
- aVL, avec l’électrode du membre supérieur gauche ;
- aVF, avec l’électrode du membre inférieur gauche.
Cela nous permet de définir un certain nombre de territoires :
- un sus-décalage en V1, V2, V3 et V4 nous donne un territoire antéro-septal, c’est-à-dire la partie antérieure du cœur et le septum interventriculaire qui est la paroi entre le ventricule gauche et le droit ;
- un sus-décalage en V5, V6, DI et aVL désigne le territoire latéral, c’est-à-dire la partie du cœur la plus à gauche, voire l’apex (la pointe) ;
- un sus-décalage en DII, DIII et aVF indique un SCA dans le territoire inférieur, en bas du cœur.
Ce sont les trois territoires principaux. Sur un ECG 18 dérivations, on peut rajouter le territoire droit qui correspond à V1, V3R, V4R et aVR et le territoire postérieur qui correspond à V7, V8 et V9.
Or, une bonne connaissance du réseau coronaire nous permet de savoir quelle artère, ou quelle branche d’artère, vascularise quel territoire et donc, en fonction du territoire sus-décalé, de savoir quelle artère est atteinte.
- le territoire antéro-septal est vascularisé par l'interventriculaire antérieure, une branche importante de la coronaire gauche ;
- le territoire latéral est vascularisé par la circonflexe ou la marginale, deux branches de la coronaire gauche ;
- le territoire inférieur est vascularisé par la circonflexe (branche de la coronaire gauche) ou par la coronaire droite ;
- les territoires droit et postérieur sont vascularisés par la coronaire droite.
L'ECG est donc très intéressant puisqu’au-delà de permettre le diagnostic, il nous permet un premier repérage sur l’artère atteinte. Toutefois, pour assurer le succès de l’opération, il va falloir recourir à des moyens un peu plus invasifs.
Coronarographie et angioplastie
Notre patient arrive en USIC, son état est inchangé et nous avons veillé à lui faire faire le moins d’effort possible.
Il passe immédiatement dans la salle de coronarographie (ou juste salle de coro).
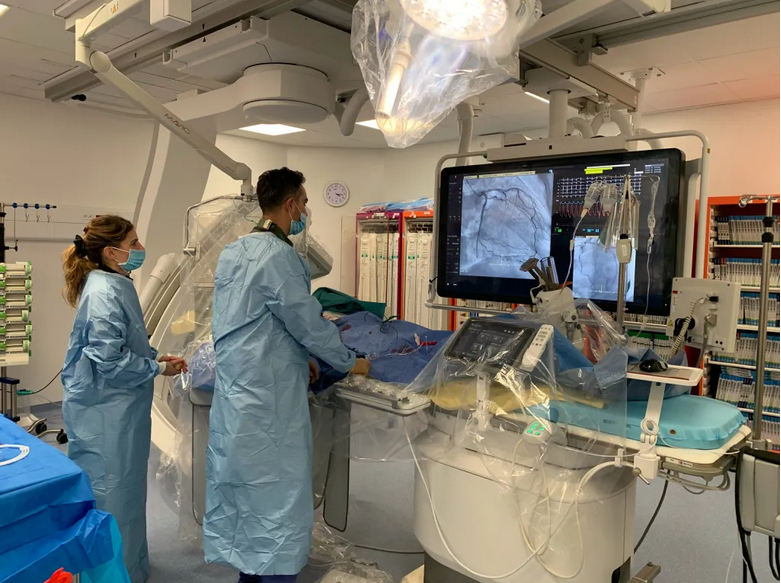
La coronarographie est un examen invasif qui permet de visualiser de manière extrêmement précise les artères coronaires et de savoir où se situent les réductions de calibre. L’opérateur (un cardiologue interventionnel) va insérer un cathéter souple dans une artère (souvent l’artère fémorale au niveau de l’aine ou l’artère radiale au niveau du poignet). Il va faire remonter ce cathéter petit à petit dans l’arbre artériel jusqu’à arriver à la sortie du cœur gauche, là où les coronaires prennent leur source. À ce moment, il va injecter dans chaque coronaire un produit de contraste. En parallèle, des clichés radios du patient sont pris en continu afin de voir la propagation du produit de contraste dans les coronaires et donc le trajet et la morphologie de celles-ci.
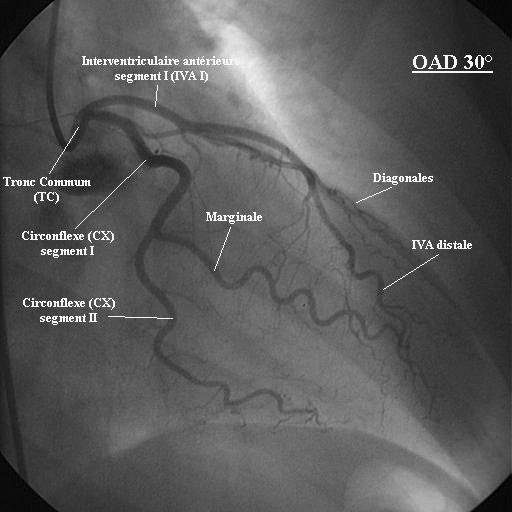
Ici l’image est normale, mais sur un examen pathologique, on repère très vite une artère dont le calibre se réduit brutalement ou qui s’arrête net. C’est là que se situe la sténose et c’est donc là qu’il va falloir intervenir.
Dans le même temps opératoire, le cardiologue va effectuer une angioplastie. Il s’agit de monter un ballonnet dégonflé sur le guide pour l’amener jusqu’à l’endroit où se situe la sténose et gonfler le ballon pour redilater l’artère en écrasant la plaque d’athérome et le thrombus.
Dans certains cas, quand le cardiologue estime que l’artère est à risque de se reboucher rapidement, il va procéder dans le même temps à la pose d’un stent. Il s’agit d’un genre de ressort métallique placé au niveau de la sténose redilatée pour la garder ouverte.
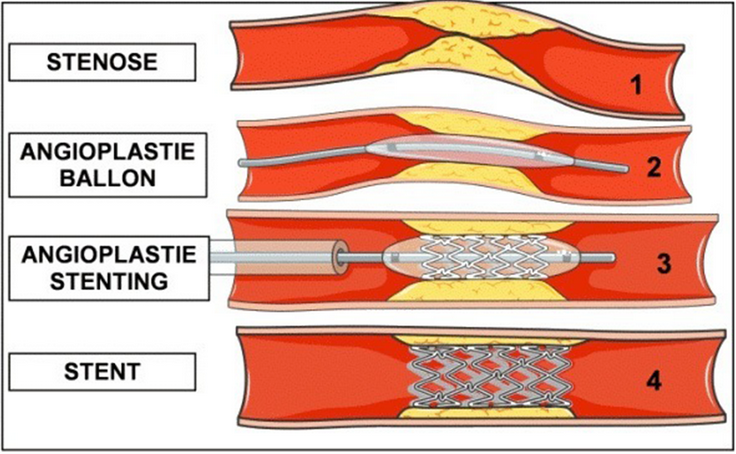
L’angioplastie n’est pas toujours possible. En effet, selon où vous habitez, il se peut que le plateau technique de coronarographie soit à plus de 2h de trajet et dans ce cas, devant l’urgence, on procède plutôt à une fibrinolyse. On injecte directement en artériel un produit qui va dissoudre le caillot. Le taux de réussite de la fibrinolyse est plus faible que celui de l’angioplastie, mais elle est plus facile à mettre en place. En cas d’échec de la fibrinolyse, on roule aussitôt à toute vitesse vers la salle de coro la plus proche pour procéder à une angioplastie de sauvetage.
L’intervention est terminée, elle ne dure que quelques minutes. Le patient va maintenant devoir être surveillé quelques jours en USIC puis en hospitalisation standard de cardiologie pour vérifier qu’il supporte bien son opération et qu’il n’y a pas de récidive.
La prise en charge totale depuis l’appel au 15 jusqu’à l’angioplastie aura duré moins d’une heure et demie, ce qui est très rapide même dans le cadre d’une urgence.
Ainsi, la prise en charge d’un SCA est une urgence qui nécessite la coopération de plusieurs services : la plateforme téléphonique, les secouristes, le SMUR et la cardiologie interventionnelle pour que tout se mette en place le plus vite possible. Au-delà du risque important d’arrêt cardiaque, chaque minute qui passe provoque de nouvelles lésions irréversibles au niveau du myocarde et fait risquer au patient une insuffisance cardiaque consécutive à son infarctus. On parle alors d'insuffisance cardiaque ischémique (l’ischémie étant le phénomène de manque de sang dans un organe).
Dans la plupart des cas toutefois, si la réaction est rapide, les séquelles seront minimes, permettant aux acteurs de la chaîne de secours de se dire - et ce n’est pas si fréquent qu’on pourrait le croire - qu’ils ont vraiment sauvé une vie.
Alors, vous avez compris l’icône ? Il s’agit tout simplement d’une angioplastie que l’on reconnaît au ballon au bout du guide qui se déplace dans une artère !
Un grand merci à @Arius pour la validation !
Sources
- Anatomie cardiaque : Anatomie Clinique, Tome 3, Thorax et Abdomen, par Kamina, Éditions Maloine.
- Physiologie cardiaque : Biologie et pathologie du cœur et des vaisseaux, 3e Édition, par la Société Française de Cardiologie, Éditions John Libbey.
- Prise en charge du SCA : Médecine Cardiovasculaire, 2e édition, R2C, par le Collège National des Enseignants de Cardiologie et la Société Française de Cardiologie, éditions Elsevier.